Hvis vand H2O er polært og ilt O2 ikke-polært, hvordan kan der være opløst i vand?
Her er grunden til, at ilt opløses i vand, selvom de har forskellige polariteter:
* delvis opløselighed: Oxygen er ikke meget opløselig i vand, men det opløses i lille grad. Dette skyldes, på trods af at være ikke-polært, ilt kan interagere med vandmolekyler gennem svage van der Waals-styrker. Disse kræfter er midlertidige attraktioner, der opstår fra udsving i elektronfordeling inden for molekyler. Mens svagere end brintbindinger (den primære interaktion mellem vandmolekyler), giver de stadig en vis grad af interaktion og opløsning.
* Temperatur: Oxygenopløselighed i vand er temperaturafhængig . Koldt vand kan indeholde mere opløst ilt end varmt vand. Dette skyldes, at når temperaturen stiger, bevæger vandmolekylerne sig hurtigere, hvilket gør det vanskeligere for ilt at danne disse svage interaktioner og forblive opløst.
* tryk: Forøgelse af ilttrykket over vandet øger også dens opløselighed. Dette skyldes, at højere tryk kræfter flere iltmolekyler i vandet og overvinder modstanden fra de svagere van der Waals -styrker.
Kortfattet: Mens ilt og vand har forskellige polariteter, kan ilt stadig opløses i vand i et begrænset omfang på grund af svage van der Waals kræfter, påvirket af temperatur og tryk.
Vigtig note: Oxygenes opløselighed i vand er afgørende for akvatisk liv. Fisk og andre akvatiske organismer er afhængige af opløst ilt til respiration. Faktorer som temperatur og forurening kan påvirke iltniveauer i vand, hvilket fører til negative indvirkninger på akvatiske økosystemer.
Sidste artikelHvordan dannes en brintbinding?
Næste artikelHvad er oxidation og forklare denne proces?
 Varme artikler
Varme artikler
-
 Kemikere udvikler nyt materiale, der hjælper smart glas med at skifte farve på rekordtidFarveændring i elektrokrome materialer. Kredit:© Vera Hiendl, e-konvertering / LMU Smart glas kan ændre farve hurtigt gennem elektricitet. Et nyt materiale udviklet af kemikere fra Ludwig-Maximili
Kemikere udvikler nyt materiale, der hjælper smart glas med at skifte farve på rekordtidFarveændring i elektrokrome materialer. Kredit:© Vera Hiendl, e-konvertering / LMU Smart glas kan ændre farve hurtigt gennem elektricitet. Et nyt materiale udviklet af kemikere fra Ludwig-Maximili -
 Nye metamaterialer omdannes til nye former, overtager nye ejendommeEt nanoarchitected metamateriale deformerer for at oprette Caltech -ikonet. Kredit:Julia Greer/Caltech En nyudviklet type arkitekteret metamateriale har evnen til at ændre form på en afstemt måde.
Nye metamaterialer omdannes til nye former, overtager nye ejendommeEt nanoarchitected metamateriale deformerer for at oprette Caltech -ikonet. Kredit:Julia Greer/Caltech En nyudviklet type arkitekteret metamateriale har evnen til at ændre form på en afstemt måde. -
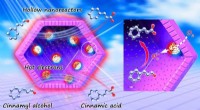 Konstruktion af hule nanoreaktorer til forbedrede fotooxidationerSkematisk diagram af hule nanoreaktorer til fotokatalytisk oxidation af cinnamylalkohol. Kredit:Science China Press Oxidation af primære alkoholer til carboxylsyrer er af betydning i både organisk
Konstruktion af hule nanoreaktorer til forbedrede fotooxidationerSkematisk diagram af hule nanoreaktorer til fotokatalytisk oxidation af cinnamylalkohol. Kredit:Science China Press Oxidation af primære alkoholer til carboxylsyrer er af betydning i både organisk -
 Indbygget gassensorenhed lover enkel, nøjagtig påvisning af flygtige organiske forbindelserI gennemgang af videnskabelige instrumenter, forskere ved Gdańsk University of Technology beskriver en måleanordning designet til at analysere luftprøver indeholdende forskellige flygtige organiske fo
Indbygget gassensorenhed lover enkel, nøjagtig påvisning af flygtige organiske forbindelserI gennemgang af videnskabelige instrumenter, forskere ved Gdańsk University of Technology beskriver en måleanordning designet til at analysere luftprøver indeholdende forskellige flygtige organiske fo
- Hvad gør en forklaring god nok?
- Hvad betyder satellitbillede?
- 10 gange bekæmpede menneskeheden mod naturen (og vandt)
- Ny bioink bringer 3D-print af menneskelige organer tættere på virkeligheden
- Hvad er 2 kontinenter, der vi vippede fuldstændigt mod solen i juli?
- Hvordan kan du tegne et energioverførselsdiagram til et fyrværkeri?


