Er ammoniumfluorid polært eller ikke polært?
* molekylær form: Ammoniumionen (NH₄⁺) har en tetrahedral form på grund af de fire hydrogenatomer bundet til nitrogenatomet. Fluorionionen (F⁻) er et enkelt atom.
* Elektronegativitet: Fluor er det mest elektronegative element, hvilket betyder, at det tiltrækker elektroner stærkere end nitrogen eller brint. Dette skaber en signifikant forskel i elektronegativitet mellem nitrogen- og fluoratomer i ammoniumfluoridmolekylet.
* dipolmoment: Den ulige deling af elektroner mellem nitrogen- og fluoratomer skaber en delvis negativ ladning på fluoratomet og en delvis positiv ladning på nitrogenatomet. Dette skaber et dipolmoment, hvilket indikerer en adskillelse af ladning inden for molekylet.
Kortfattet: Den asymmetriske form af molekylet og den signifikante forskel i elektronegativitet mellem nitrogen og fluor resulterer i et netto dipolmoment, hvilket gør ammoniumfluorid til et polært molekyle.
Sidste artikelHvor mange atomer er der i 0,850 mol ammoniak?
Næste artikelHvad er et forældet navn på svovl?
 Varme artikler
Varme artikler
-
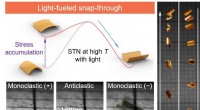 Molekylær switch muliggør fotomekanisk spring af polymererDen foto-inducerede bi-stabile struktur gør det muligt for den fotoaktive flydende krystallinske polymer at opnå snap-through inspireret spring. Effektiv fotoinduceret energiakkumulering og frigivelse
Molekylær switch muliggør fotomekanisk spring af polymererDen foto-inducerede bi-stabile struktur gør det muligt for den fotoaktive flydende krystallinske polymer at opnå snap-through inspireret spring. Effektiv fotoinduceret energiakkumulering og frigivelse -
 Forskere udvikler klæbemiddel med industriel styrke, som kan løsnes i magnetfeltetKredit:CC0 Public Domain Forskere ved University of Sussex har udviklet en lim, som kan løsne sig, når den placeres i et magnetfelt, dvs. produkter, der ellers er bestemt til deponering, kunne nu
Forskere udvikler klæbemiddel med industriel styrke, som kan løsnes i magnetfeltetKredit:CC0 Public Domain Forskere ved University of Sussex har udviklet en lim, som kan løsne sig, når den placeres i et magnetfelt, dvs. produkter, der ellers er bestemt til deponering, kunne nu -
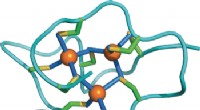 Heavy metal-bindingsdomæne i et cystein-rigt protein kan være havsneglstilpasning til metalspændi…Strukturel tilpasning af et protein til øget metalspænding:NMR -struktur af en marin snegl Metallothionein med et ekstra domæne. Kredit:Wiley En særlig type af små svovlrige proteiner, metallothio
Heavy metal-bindingsdomæne i et cystein-rigt protein kan være havsneglstilpasning til metalspændi…Strukturel tilpasning af et protein til øget metalspænding:NMR -struktur af en marin snegl Metallothionein med et ekstra domæne. Kredit:Wiley En særlig type af små svovlrige proteiner, metallothio -
 Forskere forbedrer katalysatoren, der ødelægger kemikalier for evigt med sollysIllustration, der viser, hvordan et kompositmateriale indeholdende plader af bornitrid (gitter af blå og sølvkugler) og nanopartikler af titaniumdioxid (grå kugler) bruger langbølget ultraviolet energ
Forskere forbedrer katalysatoren, der ødelægger kemikalier for evigt med sollysIllustration, der viser, hvordan et kompositmateriale indeholdende plader af bornitrid (gitter af blå og sølvkugler) og nanopartikler af titaniumdioxid (grå kugler) bruger langbølget ultraviolet energ
- Hvad er planeterne i alfibetisk rækkefølge?
- Hvad er formlerne til lithiumcarbonatvarme?
- Hvorfor salatens mitokondrielle genom er som en hakket salat
- Hvis dit tv talte til dig, ville du så købe det? Undersøgelse finder, at folk bruger mere på nog…
- Hvad er det, at atomer af materialer udfører elektricitet bedst at blive holdt sammen af?
- Hvorfor er kraft ikke en scaler-mængde?


