Har cesium højere eller lavere smeltepunkter end natrium, og hvorfor?
* Metallisk binding: Både cesium og natrium er alkalimetaller og udviser metallisk binding. Ved metallisk binding delokaliseres elektroner og danner et "hav" af elektroner, der holder de positivt ladede metalioner sammen.
* atomstørrelse: Cesium er markant større end natrium. Denne større størrelse betyder, at de ydre elektroner er længere væk fra kernen og oplever svagere tiltrækning.
* Elektrostatisk attraktion: Den svagere tiltrækning mellem kernen og de ydre elektroner i cæsium fører til svagere metallisk binding.
* smeltepunkt: Svagere metallisk binding oversættes til et lavere smeltepunkt. Det kræver mindre energi for at bryde bindingerne og smelte metallet.
Kortfattet: Den større atomstørrelse og svagere metallisk binding i cæsium fører til et lavere smeltepunkt sammenlignet med natrium.
Sidste artikelNår flydende vand udsættes for 32 Ferinheight det?
Næste artikelHvilket element findes i en forbindelse kaldet Bauxite?
 Varme artikler
Varme artikler
-
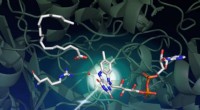 Forskere afdækker strukturen af lysdrevet enzym med potentielle anvendelser af biobrændstofEn undersøgelse med SLACs LCLS røntgenlaser fangede, hvordan lys driver en række komplekse strukturelle ændringer i et enzym kaldet FAP, som katalyserer omdannelsen af fedtsyrer til udgangsbestandde
Forskere afdækker strukturen af lysdrevet enzym med potentielle anvendelser af biobrændstofEn undersøgelse med SLACs LCLS røntgenlaser fangede, hvordan lys driver en række komplekse strukturelle ændringer i et enzym kaldet FAP, som katalyserer omdannelsen af fedtsyrer til udgangsbestandde -
 Ny isomerseparationsmetode er en velsignelse for forskning i proteinoxidationKemikere ved UC Santa Cruz rapporterede om en ny metode til adskillelse af methioninsulfoxiddiastereomerer, der åbner nye muligheder for at studere deres roller i biologiske processer. Kredit:Omslagsk
Ny isomerseparationsmetode er en velsignelse for forskning i proteinoxidationKemikere ved UC Santa Cruz rapporterede om en ny metode til adskillelse af methioninsulfoxiddiastereomerer, der åbner nye muligheder for at studere deres roller i biologiske processer. Kredit:Omslagsk -
 Hvordan teknologi designet til det ydre rum kan hjælpe med at opdage sygdomme på planeten JordenKredit:Kings College London Sepsis, en livstruende tilstand, hvor kroppen bekæmper en alvorlig infektion, der har spredt sig via blodbanen, hvilket fører til dårlig cirkulation og manglende blodge
Hvordan teknologi designet til det ydre rum kan hjælpe med at opdage sygdomme på planeten JordenKredit:Kings College London Sepsis, en livstruende tilstand, hvor kroppen bekæmper en alvorlig infektion, der har spredt sig via blodbanen, hvilket fører til dårlig cirkulation og manglende blodge -
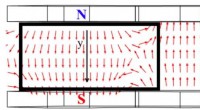 Magnetfelters indflydelse på tyndfilmstrukturerVisualisering af et magnetfelt mellem permanente magneter ved placeringen af substratet til aflejring af NiFe/IrMn film tyndfilmstruktur. Kredit:Valeria Rodionova Et team af forskere fra Immanue
Magnetfelters indflydelse på tyndfilmstrukturerVisualisering af et magnetfelt mellem permanente magneter ved placeringen af substratet til aflejring af NiFe/IrMn film tyndfilmstruktur. Kredit:Valeria Rodionova Et team af forskere fra Immanue


