Hvad er de mest sandsynlige anklager for ioner dannet af barium og nitrogen?
* barium (BA): Barium er i gruppe 2 i den periodiske tabel, hvilket betyder, at den har 2 valenselektroner. Det har en tendens til at miste disse to elektroner for at opnå en stabil octet, der danner en +2 ion (ba²⁺).
* nitrogen (n): Nitrogen er i gruppe 15 i den periodiske tabel, hvilket betyder, at det har 5 valenselektroner. Det har en tendens til at vinde 3 elektroner for at opnå en stabil octet, der danner en -3 -ion (n³⁻).
Derfor er de mest sandsynlige anklager for ioner dannet fra barium og nitrogen:
* barium:ba²⁺
* nitrogen:n³⁻
Sidste artikelHvad sker der, når et stof skifter fra fast til væske?
Næste artikelBalance denne ligning CH4 plus O2 er lig med CO2 H2O?
 Varme artikler
Varme artikler
-
 Sikker løsning til at opsuge oliespildKredit:CC0 Public Domain Der har været mere end 700 olieudslip på verdensplan i de sidste 20 år, forurenende have og kyststrækninger samt fare for marin økologi og andet dyreliv. Lektor Jingsan X
Sikker løsning til at opsuge oliespildKredit:CC0 Public Domain Der har været mere end 700 olieudslip på verdensplan i de sidste 20 år, forurenende have og kyststrækninger samt fare for marin økologi og andet dyreliv. Lektor Jingsan X -
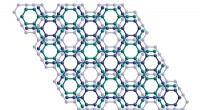 Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved
Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved -
 Ny belægningsproces giver effektiv beskyttelse af bremseskiverBelægning af en bremseskive med EHLA-processen. Kredit:Fraunhofer ILT, Aachen, Tyskland / Volker Lannert Mere end mange andre bildele, bremseskiver udsættes for gentagne mekaniske belastninger. So
Ny belægningsproces giver effektiv beskyttelse af bremseskiverBelægning af en bremseskive med EHLA-processen. Kredit:Fraunhofer ILT, Aachen, Tyskland / Volker Lannert Mere end mange andre bildele, bremseskiver udsættes for gentagne mekaniske belastninger. So -
 Forskere afslører dynamisk sølvkrystallisering ved in-situ SEMRadikale fluktuationer fører til sølv dynamisk krystallisation i et in-situ scanning elektronmikroskop. Kredit:HAN Yongsheng Forskellige strukturerede materialer har forskellige egenskaber og anve
Forskere afslører dynamisk sølvkrystallisering ved in-situ SEMRadikale fluktuationer fører til sølv dynamisk krystallisation i et in-situ scanning elektronmikroskop. Kredit:HAN Yongsheng Forskellige strukturerede materialer har forskellige egenskaber og anve
- Kulstofmarked kan opveje Australiens enorme regning for genopretning af brand
- Er vibrationer en cirkulær bevægelse ja eller nej?
- Hvad er målet for antiknock -egenskaber i et brændstof?
- Registrering af fødslen af en nanoplasma
- Arsenrisikoen i Pakistan er meget større end forventet
- Hvor meget arbejde udføres af en kraft 10n til at flytte et objekt gennem afstand 1 m i retning af …


