Beregn masse på 3,011 x 10 23 Ingen nitrogenatomer?
forståelse af konceptet
* avogadros nummer: 6,022 x 10^23 er Avogadros nummer, der repræsenterer antallet af atomer eller molekyler i en mol af et stof.
* molmasse: Den molære masse af nitrogen (N) er 14,01 g/mol. Dette betyder, at en mol nitrogenatomer vejer 14,01 gram.
Beregning
1. Find antallet af mol:
* Opdel det givne antal atomer med Avogadros nummer:
(3.011 x 10^23 atomer) / (6.022 x 10^23 atomer / mol) =0,5 mol
2. Beregn massen:
* Multiplicer antallet af mol med den molære masse:
(0,5 mol) * (14,01 g/mol) = 7,005 gram
Derfor er massen på 3,011 x 10^23 nitrogenatomer 7,005 gram
Sidste artikelHvad er reaktionen af K2CR2O7 med SO2?
Næste artikelReaktion af brintchloridgas med vand?
 Varme artikler
Varme artikler
-
 Oprydning af CO2 -emissioner kan være millioner værdSkematisk fremstilling af en mulig fremtidig C2CNT-station, der bruger solvarmeenergi til at omdanne kuldioxid fra atmosfæren til kulstof nanorøruld. Kredit:Johnson et al. © 2017 Elsevier Ltd. (Ph
Oprydning af CO2 -emissioner kan være millioner værdSkematisk fremstilling af en mulig fremtidig C2CNT-station, der bruger solvarmeenergi til at omdanne kuldioxid fra atmosfæren til kulstof nanorøruld. Kredit:Johnson et al. © 2017 Elsevier Ltd. (Ph -
 Ny, glat toiletbelægning giver renere skylning, sparer vandPenn State forskere har udviklet en metode, der dramatisk reducerer mængden af vand, der er nødvendig for at skylle et konventionelt toilet, som normalt kræver 6 liter. Kredit:Wong Laboratory for Na
Ny, glat toiletbelægning giver renere skylning, sparer vandPenn State forskere har udviklet en metode, der dramatisk reducerer mængden af vand, der er nødvendig for at skylle et konventionelt toilet, som normalt kræver 6 liter. Kredit:Wong Laboratory for Na -
 Forskere udvikler billige, drop-on-demand printteknikDrop impact printopsætning med genbrugsenhed. Kredit:Nature Communications, Laboratorium for mikrofluidiske enheder og heterogene systemer, CeNSE Forskere ved Center for Nano Science and Engineeri
Forskere udvikler billige, drop-on-demand printteknikDrop impact printopsætning med genbrugsenhed. Kredit:Nature Communications, Laboratorium for mikrofluidiske enheder og heterogene systemer, CeNSE Forskere ved Center for Nano Science and Engineeri -
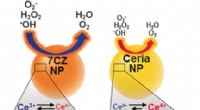 Ceria-zirconia nanopartikler som forbedrede multi-antioxidanter er effektive til behandling af sepsi…Kredit:Wiley Under sepsis, celler er oversvømmet med reaktive iltarter, der genereres i et afvigende respons fra immunsystemet på en lokal infektion. Hvis denne fatale inflammatoriske vej kunne fo
Ceria-zirconia nanopartikler som forbedrede multi-antioxidanter er effektive til behandling af sepsi…Kredit:Wiley Under sepsis, celler er oversvømmet med reaktive iltarter, der genereres i et afvigende respons fra immunsystemet på en lokal infektion. Hvis denne fatale inflammatoriske vej kunne fo
- Olieprisstyrt:vil det påvirke overgangen til grøn energi?
- Ingeniører løser katalyse vs korrosionsmysterium i elektrokemisk ozonproduktion
- Hvad skal der til for at finde liv på Venus?
- Hvordan nyfødte stjerner forbereder sig på fødslen af planeter
- Kortlægning af Venus:Ekstrem makeover eller pladetektonik?
- AT&T idømte en bøde på 60 millioner dollars for vildledning med ubegrænsede planer


