Hvordan adskiller de ændringer, der opstår, når vand blandes med salt, fra resultatet natrium?
Vand og salt (NaCl):
* opløsning: Når salt tilsættes til vand, opløses det. Dette betyder, at de ioniske bindinger, der holder natrium (Na+) og chlorid (Cl-) -ioner sammen i saltkrystallen, er brudt. Vandmolekylerne, der er polære, omgiver ionerne og trækker dem fra hinanden.
* Ingen kemisk reaktion: Der er ingen kemisk reaktion mellem salt og vand. Salt opløses simpelthen i dets bestanddele og danner en elektrolytopløsning.
* Resultat: Du får en homogen opløsning af salt opløst i vand. Løsningen er salt, men den kemiske sammensætning af vandet og salt forbliver uændret.
vand og natriummetal (NA):
* voldelig kemisk reaktion: Når natriummetal tilsættes til vand, forekommer en meget eksoterm (varmefrigivende) kemisk reaktion.
* Dannelse af natriumhydroxid og brintgas: Natrium reagerer med vand for at producere natriumhydroxid (NaOH), en stærk base og brintgas (H2). Reaktionen er repræsenteret af følgende ligning:
2NA (S) + 2H₂O (L) → 2NAOH (AQ) + H₂ (G)
* varme og eksplosion: Reaktionen er ekstremt hurtig, hvilket genererer betydelig varme og fører ofte til en eksplosion. Den producerede brintgas er brandfarlig og kan antænde i nærvær af luft.
* Resultat: Du får en opløsning af natriumhydroxid (LYE) og brintgas. Natriummetallet forbruges fuldstændigt i reaktionen.
Nøgleforskelle:
* kemisk reaktion vs. opløsning: Salt opløses i vand, mens natrium reagerer kemisk med vand.
* slutprodukter: Blanding af salt med vand resulterer i en opløsning af ioner. Blanding af natrium med vand producerer natriumhydroxid og brintgas.
* fare: Det er ekstremt farligt at blande natrium med vand på grund af den voldelige reaktion og potentiale for eksplosion. Blanding af salt med vand er generelt sikkert.
I det væsentlige opløses salt i vand og danner en opløsning af ioner, mens natrium reagerer med vand og producerer nye kemiske forbindelser.
Sidste artikelHvordan tilberedes brint i laboratoriet?
Næste artikelHvad er Valency of Carbon?
 Varme artikler
Varme artikler
-
 Video—Vinsnobberi:Fakta vs. fiktionKredit:The American Chemical Society Vi kender alle mindst én vinsnob, der gennemgår alle mulige ritualer, som de sværger vil bringe den bedste smag frem, som at hvirvle glasset og dekantere flask
Video—Vinsnobberi:Fakta vs. fiktionKredit:The American Chemical Society Vi kender alle mindst én vinsnob, der gennemgår alle mulige ritualer, som de sværger vil bringe den bedste smag frem, som at hvirvle glasset og dekantere flask -
 Video:De eksplosive konsekvenser af ko bøvserKredit:The American Chemical Society Køer bøvser mere gas, end du måske tror muligt, når de fordøjer græs. Det meste af den gas er metan, en potent drivhusgas, hvilket er dårlige nyheder for plan
Video:De eksplosive konsekvenser af ko bøvserKredit:The American Chemical Society Køer bøvser mere gas, end du måske tror muligt, når de fordøjer græs. Det meste af den gas er metan, en potent drivhusgas, hvilket er dårlige nyheder for plan -
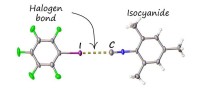 Ny ikke -kovalent binding blokerer frastødende lugt af isocyaniderStrukturen af associerede iodopentafluorobensen med mesityl isocyanid, etableret ved røntgendiffraktion ved Research Park ved St. Petersburg State University. Kredit:SPbU Isocyanider er en vigti
Ny ikke -kovalent binding blokerer frastødende lugt af isocyaniderStrukturen af associerede iodopentafluorobensen med mesityl isocyanid, etableret ved røntgendiffraktion ved Research Park ved St. Petersburg State University. Kredit:SPbU Isocyanider er en vigti -
 En corny løsning til at hjælpe med at bekæmpe spredningen af den nye coronavirusKarakteristisk for denne håndsprit kommer fra dens ethanolbase. Ethanol er en plantebaseret vedvarende energikilde-i USA primært fremstillet af majs-der ofte blandes med benzin til køretøjer. Kredit:U
En corny løsning til at hjælpe med at bekæmpe spredningen af den nye coronavirusKarakteristisk for denne håndsprit kommer fra dens ethanolbase. Ethanol er en plantebaseret vedvarende energikilde-i USA primært fremstillet af majs-der ofte blandes med benzin til køretøjer. Kredit:U
- Hvor mange mol C er i 1,22 C6H12O6?
- Er jorden i ørken frugtbar?
- Sådan fungerer hørelsen
- Forskere bekræfter, at folk dømmer hele grupper baseret på dets første medlems præstationer
- En pålidelig eksperimentel benchmark i krystalstruktur forudsigelse af farmaceutiske lægemidler
- Ny DNA-baseret chip kan programmeres til at løse komplekse matematiske problemer


