Hvor mange liter svovldioxid produceres fra reaktionen med 26,9 L ilt?
Her er hvorfor:
* støkiometri: Den afbalancerede kemiske ligning fortæller os molforholdene mellem reaktanter og produkter.
* Ideel gaslov: For at relatere liter (volumen) til mol bruger vi den ideelle gaslov (PV =NRT).
Eksempel:
Lad os sige, at reaktionen er:
S + O₂ → SO₂
Dette betyder, at 1 mol svovl reagerer med 1 mol ilt for at producere 1 mol svovldioxid.
trin til at løse:
1. Balance ligningen: Ligningen er allerede afbalanceret.
2. Konverter liter ilt til mol: Ved hjælp af den ideelle gaslov skal du kende iltgasens temperatur og tryk for at beregne antallet af mol.
3. Brug molforholdet: Den afbalancerede ligning viser, at 1 mol ilt producerer 1 mol svovldioxid.
4. Konverter mol svovldioxid til liter: Igen har du brug for temperaturen og trykket for at bruge den ideelle gaslov til at beregne volumen i liter.
Angiv den kemiske reaktion og temperatur- og trykbetingelserne, så jeg kan hjælpe dig med at beregne literne produceret svovldioxid.
Sidste artikel24 g ch4 reagerer med 96 g o2?
Næste artikelHvilken ædel gas ville sandsynligvis danne en forbindelse med fluor?
 Varme artikler
Varme artikler
-
 Frysrammemikroskopi indfanger molekyler, der låses og belastes af DNATranskriptionsfaktor IID -komplekset låser sig på DNA, kontrollerer, at det er det rigtige sted og rekrutterer derefter andre proteiner til at begynde at transkribere DNA til RNA. Nye fremskridt inden
Frysrammemikroskopi indfanger molekyler, der låses og belastes af DNATranskriptionsfaktor IID -komplekset låser sig på DNA, kontrollerer, at det er det rigtige sted og rekrutterer derefter andre proteiner til at begynde at transkribere DNA til RNA. Nye fremskridt inden -
 Fotokatalytiske nanofibre udviklet til brug i effektiv brintproduktionKredit:CC0 Public Domain Et team af forskere fra Storbritannien, Canada og Hong Kong har udviklet fotokatalytiske nanofibre, der kan bruges til effektiv produktion af brint. I deres papir offentli
Fotokatalytiske nanofibre udviklet til brug i effektiv brintproduktionKredit:CC0 Public Domain Et team af forskere fra Storbritannien, Canada og Hong Kong har udviklet fotokatalytiske nanofibre, der kan bruges til effektiv produktion af brint. I deres papir offentli -
 Blæksprutteskind inspirerer til skabelsen af næste generations rumtæppeAlon Gorodetsky, UCI lektor i kemisk og biomolekylær teknik, og Erica Leung, en UCI kandidatstuderende i den afdeling, har opfundet et nyt materiale, der kan fange eller frigive varme efter ønske. Kre
Blæksprutteskind inspirerer til skabelsen af næste generations rumtæppeAlon Gorodetsky, UCI lektor i kemisk og biomolekylær teknik, og Erica Leung, en UCI kandidatstuderende i den afdeling, har opfundet et nyt materiale, der kan fange eller frigive varme efter ønske. Kre -
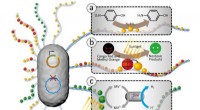 Konstruerede bakterielle biofilm, der immobiliserer nanopartikler, muliggør forskellige katalytiske…Forskellige katalytiske anvendelser af tunable funktionel E coli biofilm med forankrede nanoobjekter. (a) De biofilmforankrede Au NPer muliggør den genanvendelige katalytiske reduktion af den giftig
Konstruerede bakterielle biofilm, der immobiliserer nanopartikler, muliggør forskellige katalytiske…Forskellige katalytiske anvendelser af tunable funktionel E coli biofilm med forankrede nanoobjekter. (a) De biofilmforankrede Au NPer muliggør den genanvendelige katalytiske reduktion af den giftig
- Jo mere molekylerne et objekt indeholder varmeenergi, den har?
- Intron: Definition, funktion og betydning i RNA-splejsning
- Jetliner lander i USA efter verdens længste flyvning
- Ny open source-software forudsiger virkningerne af ekstreme begivenheder på net
- Swarm afslører, hvorfor GPS -satellitter mister overblikket over ækvator mellem Afrika og Sydameri…
- Madras brændbarhedsstandard er en livredder, NIST-rapport finder


