I hvilken gruppe danner elementerne normalt, at chlorider har formler, der slutter i CL2?
Her er hvorfor:
* Valenselektroner: Alkaliske jordmetaller har to valenselektroner.
* ionisk binding: De har en tendens til at miste disse to elektroner til dannelse af +2 kationer.
* klor: Chlor, et halogen, får en elektron til dannelse af en -1 -anion (Cl⁻).
* afbalanceringsafgifter: For at opnå en neutral forbindelse er der behov for to chlorioner (2 x cl⁻ =-2 ladning) for at afbalancere +2 ladning af den alkaliske jordmetalkation.
Eksempler:
* calciumchlorid (cacl₂): Ca²⁺ + 2Cl⁻ → Cacl₂
* magnesiumchlorid (MGCL₂): Mg²⁺ + 2Cl⁻ → Mgcl₂
Vigtig note: Mens de fleste alkaliske jordmetaller danner chlorider med CL₂ -formlen, findes der nogle undtagelser. For eksempel er berylliumchlorid (becl₂) en kovalent forbindelse, og dens formel er becl₂.
Sidste artikelHvad er betingelserne for, at ammoniakmolekyle skal være IR -aktive?
Næste artikelHvad er formlen for bly 2 hydroxid?
 Varme artikler
Varme artikler
-
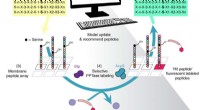 Brug af maskinlæring til at designe peptiderOversigt over den iterative Peptid Optimering med Optimal Learning (POOL) metode workflow. Kredit: Naturkommunikation (2018). DOI:10.1038/s41467-018-07717-6 Forskere og ingeniører har længe været
Brug af maskinlæring til at designe peptiderOversigt over den iterative Peptid Optimering med Optimal Learning (POOL) metode workflow. Kredit: Naturkommunikation (2018). DOI:10.1038/s41467-018-07717-6 Forskere og ingeniører har længe været -
 Undersøgelse identificerer æteriske olieforbindelser, der er mest giftige for væggelusKredit:Charles Rondeau/public domain De syntetiske pesticider, der bruges til at bekæmpe væggelusangreb, står over for to problemer:insekterne får en tolerance over for dem, og mange forbrugere le
Undersøgelse identificerer æteriske olieforbindelser, der er mest giftige for væggelusKredit:Charles Rondeau/public domain De syntetiske pesticider, der bruges til at bekæmpe væggelusangreb, står over for to problemer:insekterne får en tolerance over for dem, og mange forbrugere le -
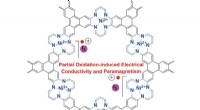 Nye 2-D metal organiske rammer med interessant elektrisk ledningsevne og magnetiske egenskaberFigur 1. Kemisk struktur af jod-dopet Ni (II) tetraaza [14] annulenbundet MOF (NiTAA-MOF). Mens NiTAA-MOF er en isolator, det oxiderede molekyle får elektrisk ledningsevne og paramagnetisme. Kredit:In
Nye 2-D metal organiske rammer med interessant elektrisk ledningsevne og magnetiske egenskaberFigur 1. Kemisk struktur af jod-dopet Ni (II) tetraaza [14] annulenbundet MOF (NiTAA-MOF). Mens NiTAA-MOF er en isolator, det oxiderede molekyle får elektrisk ledningsevne og paramagnetisme. Kredit:In -
 Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt
Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt
- Passiv rewilding kan hurtigt udvide britisk skov uden omkostninger
- Fra gær lærer forskere, hvordan befolkninger kollapser
- Undersøgelser af fortiden tyder på, at Jordens regnbælter kan flytte sig længere mod nord
- Hvilken pladegrænse findes Haiti på?
- Kunstig intelligens og big data giver de første globale kort over vigtige vegetationstræk
- Hvad er forskellige slags laboratorieapparater og deres betydning?


