Hvor mange mol ammomiumhydroxid er til stede i 0,475 g?
1. Find den molære masse af NH₄OH:
* N:14,01 g/mol
* H:1,01 g/mol (der er 5 hydrogenatomer)
* O:16,00 g/mol
Samlet molmasse =14,01 + (1,01 x 5) + 16,00 =35,06 g/mol
2. Brug formlen:moles =masse / molær masse
* mol =0,475 g / 35,06 g / mol
* mol ≈ 0,0136 mol
Derfor er ca. 0,0136 mol ammoniumhydroxid til stede i 0,475 g.
Sidste artikelHvad er eksempler på ilt?
Næste artikelEr hydrogenchlorid opløseligt eller uopløseligt i organiske opløsningsmidler?
 Varme artikler
Varme artikler
-
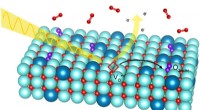 En ny facet af brændselscellekemiRøntgenstråler tillod forskere at se iltgasmolekyler klæbe til en specielt forberedt elektrodeoverflade, et vigtigt skridt i den elektrokemiske reaktion, der finder sted i brændselsceller. Kredit:Abel
En ny facet af brændselscellekemiRøntgenstråler tillod forskere at se iltgasmolekyler klæbe til en specielt forberedt elektrodeoverflade, et vigtigt skridt i den elektrokemiske reaktion, der finder sted i brændselsceller. Kredit:Abel -
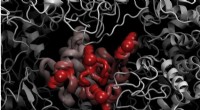 Elastisk inkohærent neutronspredning ved ILL udfordrer Lindemann-kriteriet i proteinerEt billede af lysozymproteinet, mens det smelter Proteiner er de nanomaskiner, som naturen bruger til at udføre de fleste af de processer, der er kritiske for metabolismen i celler. Et af hovedmål
Elastisk inkohærent neutronspredning ved ILL udfordrer Lindemann-kriteriet i proteinerEt billede af lysozymproteinet, mens det smelter Proteiner er de nanomaskiner, som naturen bruger til at udføre de fleste af de processer, der er kritiske for metabolismen i celler. Et af hovedmål -
 Skræddersyede enzymatiske løsninger reducerer tid og omkostninger ved bioraffinaderierKredit:MetGen Ikke mad, træagtige materialer (nemlig lignocelluloseholdig biomasse) er det største vedvarende reservoir af fermenterbar stivelse til erstatning for fossile brændstoffer. Det kan br
Skræddersyede enzymatiske løsninger reducerer tid og omkostninger ved bioraffinaderierKredit:MetGen Ikke mad, træagtige materialer (nemlig lignocelluloseholdig biomasse) er det største vedvarende reservoir af fermenterbar stivelse til erstatning for fossile brændstoffer. Det kan br -
 Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
- Hvad er energiværdien af fødevarer målt i?
- Navne på 20 berømte forskere, der bidrog til studiecellen?
- Hvordan synes DoE -forskere, at protobionter dannet?
- Strækbar, transparent grafen-metal nanotrådselektrode
- Hvad gjorde antikke egyptiske landmænd, mens nilen oversvømmede?
- Ubegrænset kapacitet i trådløse netværk med massiv MIMO


