Hvad er den empiriske formel for en forbindelse, der 40 procent svovl og 60 ilt efter vægt?
1. Antag en 100 g prøve:
* Dette gør beregninger lettere, da procenter direkte oversættes til gram.
* Du har 40 g svovl (r) og 60 g ilt (O).
2. Konverter gram til mol:
* Opdel massen af hvert element med dets molære masse:
* Mol s =40g / 32,06 g / mol =1,25 mol
* Mol O =60 g / 16,00 g / mol =3,75 mol
3. Find det enkleste forhold mellem hele nummer:
* Opdel hver molværdi med den mindste molværdi (1,25 mol i dette tilfælde):
* S:1,25 mol / 1,25 mol =1
* O:3,75 mol / 1,25 mol =3
4. Skriv den empiriske formel:
* Forholdet mellem svovl og ilt er 1:3.
* Den empiriske formel er so₃ .
Sidste artikelHvordan reagerer methylchlorid med aluminiumchlorid?
Næste artikelHvor mange mol carbon er i 1,271 gram ethanol?
 Varme artikler
Varme artikler
-
 Infrarød sensor som ny metode til opdagelse af lægemidlerDen infrarøde sensor blev udviklet af Klaus Gerwert (til venstre) og Jörn Güldenhaupt. Kredit:Gerd Kock Ved hjælp af en infrarød sensor, biofysikere ved Ruhr-Universität Bochum (RUB) er lykkedes h
Infrarød sensor som ny metode til opdagelse af lægemidlerDen infrarøde sensor blev udviklet af Klaus Gerwert (til venstre) og Jörn Güldenhaupt. Kredit:Gerd Kock Ved hjælp af en infrarød sensor, biofysikere ved Ruhr-Universität Bochum (RUB) er lykkedes h -
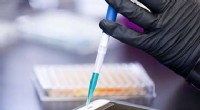 Chemist foreslår svedanalyse for bedre at sikre elektronikKemiker Jan Halámek foreslår en biometrisk-baseret tilgang til bedre at sikre elektroniske enheder. Kredit:Carlo de Jesus Jan Halámek mener, at der er en bedre metode til at sikre elektroniske enh
Chemist foreslår svedanalyse for bedre at sikre elektronikKemiker Jan Halámek foreslår en biometrisk-baseret tilgang til bedre at sikre elektroniske enheder. Kredit:Carlo de Jesus Jan Halámek mener, at der er en bedre metode til at sikre elektroniske enh -
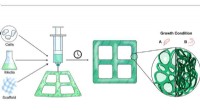 Mod tilpasset træ, dyrket i et laboratoriumI et forsøg på at levere et miljøvenligt alternativ med lavt affald, har forskere ved MIT været banebrydende med en tunbar teknik til at generere trælignende plantemateriale i et laboratorium. Kredit:
Mod tilpasset træ, dyrket i et laboratoriumI et forsøg på at levere et miljøvenligt alternativ med lavt affald, har forskere ved MIT været banebrydende med en tunbar teknik til at generere trælignende plantemateriale i et laboratorium. Kredit: -
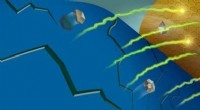 Forskere identificerer kemiske årsager til, at batterikapaciteten falmerNår manganioner (grå) fjernes fra et batteris katode (blå), de kan reagere med batteriets elektrolyt nær anoden (guld), indfangning af lithium-ioner (grøn/gul). Kredit:Robert Horn/Argonne National Lab
Forskere identificerer kemiske årsager til, at batterikapaciteten falmerNår manganioner (grå) fjernes fra et batteris katode (blå), de kan reagere med batteriets elektrolyt nær anoden (guld), indfangning af lithium-ioner (grøn/gul). Kredit:Robert Horn/Argonne National Lab
- Eksperter advarer Australien mod fare for tørke, stigende vandstand
- 200 Algeriet badende syge efter havforurening:medier
- Hvad er en mitokondrier, og hvad dens funktion?
- Den kinetiske energi af et objekt afhænger af både dets og.?
- Den bindende energi af elektroner i et metal er 178 kJ pr. Mol Hvad tærskelfrekvensen?
- Hvad hedder videnskabelig undersøgelse af menneske og menneskeheden?


