Foretager Copper LL -chlorid elektricitet i den vandige tilstand?
* ionisk forbindelse: Kobber (II) Chlorid er en ionisk forbindelse. Dette betyder, at det er sammensat af positivt ladede kobberioner (Cu²⁺) og negativt ladede chloridioner (CL⁻).
* opløsning i vand: Når Cucl₂ opløses i vand, bryder de ioniske bindinger, og ionerne bliver frie til at bevæge sig rundt i opløsningen.
* opladningsbærere: Tilstedeværelsen af disse frie, mobile ioner giver mulighed for strøm af elektrisk strøm. De positivt ladede kobberioner bevæger sig mod den negative elektrode (katode), og de negativt ladede chloridioner bevæger sig mod den positive elektrode (anode).
I resuméet skyldes kobber (II) -chloridets evne til at udføre elektricitet i den vandige tilstand dissociation af dets ioner i opløsning, hvilket giver ladningsfartsselskaber, der kan bevæge sig og bære en elektrisk strøm.
Sidste artikelHvad er den kemiske formel for rubidiumchromat?
Næste artikelHvad kan ilt og brint eksplosivt danne?
 Varme artikler
Varme artikler
-
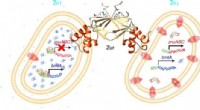 Ny indsigt i, hvordan cyanobakterier regulerer zinkoptagelsen i det åbne havKredit:Claudia Blindauer et al. Marine cyanobakterier (blågrønne alger) er væsentlige bidragsydere til det globale kulstofkredsløb og er grundlaget for fødenettet i mange af verdenshavene. De kræve
Ny indsigt i, hvordan cyanobakterier regulerer zinkoptagelsen i det åbne havKredit:Claudia Blindauer et al. Marine cyanobakterier (blågrønne alger) er væsentlige bidragsydere til det globale kulstofkredsløb og er grundlaget for fødenettet i mange af verdenshavene. De kræve -
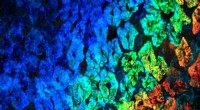 En fantastisk molekylær maskineDe adaptive iridocytter i huden på den californiske markedsblæksprutte er i stand til at indstille farven gennem det meste af spektret. Kredit:University of California - Santa Barbara blæksprutter
En fantastisk molekylær maskineDe adaptive iridocytter i huden på den californiske markedsblæksprutte er i stand til at indstille farven gennem det meste af spektret. Kredit:University of California - Santa Barbara blæksprutter -
 Tilføj bare nanomaterialer for stærkere, hårdere dykkerfinnerSpecialist i undervandsudstyr Alchemy gik sammen med Adamant Composites om at anvende nanomaterialer for at producere stærkere, hårdere kompositmateriale til dykkerfinner. Kredit:Alkymi Tilføjelse
Tilføj bare nanomaterialer for stærkere, hårdere dykkerfinnerSpecialist i undervandsudstyr Alchemy gik sammen med Adamant Composites om at anvende nanomaterialer for at producere stærkere, hårdere kompositmateriale til dykkerfinner. Kredit:Alkymi Tilføjelse -
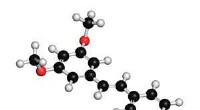 Palladiumkatalysator fremskynder to separate reaktioner, fremstilling af nyttige molekyler i en enke…Pterostilbene (billedet), et defensivt kemikalie fundet i blåbær, er et eksempel på et funktionelt molekyle, der indeholder stilben-motivet. Kredit:MOLEKUUL/SCIENCE PHOTO LIBRARY En palladiumkatal
Palladiumkatalysator fremskynder to separate reaktioner, fremstilling af nyttige molekyler i en enke…Pterostilbene (billedet), et defensivt kemikalie fundet i blåbær, er et eksempel på et funktionelt molekyle, der indeholder stilben-motivet. Kredit:MOLEKUUL/SCIENCE PHOTO LIBRARY En palladiumkatal
- Hvordan ville du beregne atommassen af atom uden at bruge periodisk tabel, hvis du kender nummerpr…
- Opdagelsen kaster lys over, hvorfor stillehavsøerne blev koloniseret
- Hvad er Jeyes Fluid?
- Hvad er en simpel maskine, der ændrer kraftretningen for at løfte et objekt?
- Ny, holdbar katalysator til nøglebrændstofcellereaktion kan vise sig nyttig i miljøvenlige køret…
- Når en masse sten og jord pludselig glider ned slop, hvad er det?


