Hvad er massen af kaliumchlorid, når 2,50 g potasium reagerer med oxidgas?
1. Skriv den afbalancerede kemiske ligning:
Reaktionen mellem kalium (K) og iltgas (O₂) producerer kaliumchlorid (KCL):
4K + O₂ → 2K₂O
2. Bestem molforholdet:
Fra den afbalancerede ligning ser vi, at 4 mol kalium reagerer med 1 mol ilt for at producere 2 mol kaliumoxid.
3. Beregn mol kalium:
* Molær masse kalium (k) =39,10 g/mol
* Mol kalium =(2,50 g) / (39,10 g / mol) =0,0639 mol
4. Beregn mol af kaliumoxid:
* Brug af molforholdet fra den afbalancerede ligning:0,0639 mol k * (2 mol k₂o / 4 mol k) =0,0320 mol k₂o
5. Beregn masse kaliumoxid:
* Molær masse kaliumoxid (K₂O) =94,20 g/mol
* Masse kaliumoxid =(0,0320 mol) * (94,20 g/mol) =3,01 g
Derfor er massen af kaliumoxid produceret, når 2,50 g kalium reagerer med iltgas, ca. 3,01 g.
 Varme artikler
Varme artikler
-
 Ny forskning identificerer styrker og svagheder ved supermaterialePolyethylen med ultrahøj molekylvægt er allerede ved at tage over fra para-aramidfibermaterialet, Kevlar, i f.eks. skudsikre jakker, som ph.d. Simon Skovsgård har på her. Kredit:Lars Kruse/AU Foto
Ny forskning identificerer styrker og svagheder ved supermaterialePolyethylen med ultrahøj molekylvægt er allerede ved at tage over fra para-aramidfibermaterialet, Kevlar, i f.eks. skudsikre jakker, som ph.d. Simon Skovsgård har på her. Kredit:Lars Kruse/AU Foto -
 En polymer kærlighedshormonsensor til tidlig påvisning af autismeSmå mængder oxytocin, en af autismens biomarkører, kan detekteres af en ny kemisk sensor, designet og fremstillet på Institute of Physical Chemistry ved det polske videnskabsakademi i Warszawa. Kred
En polymer kærlighedshormonsensor til tidlig påvisning af autismeSmå mængder oxytocin, en af autismens biomarkører, kan detekteres af en ny kemisk sensor, designet og fremstillet på Institute of Physical Chemistry ved det polske videnskabsakademi i Warszawa. Kred -
 Forskere udvikler de første lægemiddellignende forbindelser til at hæmme undvigende kræftforbund…Kredit:CC0 Public Domain Et team af forskere fra University of Michigan Rogel Cancer Center har udviklet de første lægemiddellignende forbindelser til at hæmme en nøglefamilie af enzymer, hvis fun
Forskere udvikler de første lægemiddellignende forbindelser til at hæmme undvigende kræftforbund…Kredit:CC0 Public Domain Et team af forskere fra University of Michigan Rogel Cancer Center har udviklet de første lægemiddellignende forbindelser til at hæmme en nøglefamilie af enzymer, hvis fun -
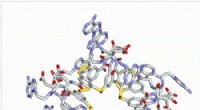 Forskere laver komplekst molekyle, der spontant folder som et proteinSet ovenfra af det centrale hulrum af det foldede molekyle. Kredit:Bin Liu, Universitetet i Groningen I biologi, foldede proteiner er ansvarlige for de fleste avancerede funktioner. Disse kompleks
Forskere laver komplekst molekyle, der spontant folder som et proteinSet ovenfra af det centrale hulrum af det foldede molekyle. Kredit:Bin Liu, Universitetet i Groningen I biologi, foldede proteiner er ansvarlige for de fleste avancerede funktioner. Disse kompleks
- Moderne alkymi skaber selvlysende jernmolekyler
- Hvorfor lægger du spole i ikke -metallisk ramme ikke metallisk ballistisk galvanometer?
- Hvilken type geologiske træk dannes, hvor to kontinentale steder kolliderer?
- Brug af computere til at åbne århundreder gamle matematiske gåder
- Hvilken type væske tillader elektricitet at passere?
- Hvorfor er der 8 planeter?


