Forklar hvorfor brint er unikt?
1. Enkleste element:
- Hydrogen har den enkleste atomstruktur, der består af kun en proton og en elektron. Dette gør det til det letteste element på den periodiske tabel.
2. Overflod:
- Hydrogen er det mest rigelige element i universet, der udgør ca. 75% af dets samlede masse. Det findes i stjerner, planeter og endda vand på jorden.
3. Alsidig reaktivitet:
- Brint kan reagere med mange andre elementer for at danne en lang række forbindelser. Det kan være både et oxiderende og reduktionsmiddel, afhængigt af reaktionen.
4. Brændstofpotentiale:
- Hydrogen betragtes som en lovende ren energikilde, da dens forbrænding kun producerer vand uden drivhusgasemissioner. Dette gør det til et potentielt alternativ til fossile brændstoffer.
5. Unik limning:
- Hydrogen kan danne usædvanlige bindinger, såsom brintbindinger, som er afgørende i biologiske systemer og kemiske reaktioner.
6. Isotoper:
- Hydrogen har tre isotoper:protium (mest almindeligt), deuterium (tungt brint) og tritium (radioaktivt). Disse isotoper har forskellige egenskaber og applikationer.
7. Kvanteadfærd:
- På grund af dens lille størrelse udviser brint betydelige kvante mekaniske effekter, hvilket gør det til et fascinerende studieemne i kvantefysik.
8. Rolle i syre-base kemi:
- Hydrogenioner (H+) spiller en grundlæggende rolle i syre-base-kemi, der bestemmer en opløsnings surhed eller grundlæggende.
9. Industrielle applikationer:
- Brint bruges i mange industrielle processer, herunder ammoniakproduktion, olieraffinering og produktion af forskellige kemikalier.
10. Medicinske applikationer:
- Deuterium og Tritium har anvendelser inden for medicinsk billeddannelse og nuklearmedicin.
Generelt gør Hydrogen's unikke egenskaber det til et vigtigt element på forskellige områder, fra astrofysik til kemi til medicin. Dets potentiale som en ren energikilde gør det også til et fokus på løbende forskning og udvikling.
Sidste artikelHvordan adskiller massetalet sig fra atom af et atom?
Næste artikelHvad er den interne struktur i et atom?
 Varme artikler
Varme artikler
-
 Nyt materiale til behandling af sår kan beskytte mod resistente bakterierForskere ved Chalmers Tekniske Universitet, Sverige, har udviklet et nyt materiale, der dræber bakterier og potentielt kan forhindre infektioner i sår - en specialdesignet hydrogel, der virker mod all
Nyt materiale til behandling af sår kan beskytte mod resistente bakterierForskere ved Chalmers Tekniske Universitet, Sverige, har udviklet et nyt materiale, der dræber bakterier og potentielt kan forhindre infektioner i sår - en specialdesignet hydrogel, der virker mod all -
 Manglende atomer i en glemt krystal bringer luminescensPerovskitten har en kraftig grøn fluorescens. Kredit:© 2017 De Bastiani Et lidet undersøgt medlem af perovskitfamilien af materialer kunne finde anvendelse i en række elektroniske enheder, efter
Manglende atomer i en glemt krystal bringer luminescensPerovskitten har en kraftig grøn fluorescens. Kredit:© 2017 De Bastiani Et lidet undersøgt medlem af perovskitfamilien af materialer kunne finde anvendelse i en række elektroniske enheder, efter -
 Neurotransmittere på et øjeblikForskning udført på IPC PAS ved hjælp af den nye forskningsmetode muliggør tidlig påvisning af neurotransmittermangler, som hjælper med at forhindre forskellige sygdomme. På billedet ses Magdalena Kun
Neurotransmittere på et øjeblikForskning udført på IPC PAS ved hjælp af den nye forskningsmetode muliggør tidlig påvisning af neurotransmittermangler, som hjælper med at forhindre forskellige sygdomme. På billedet ses Magdalena Kun -
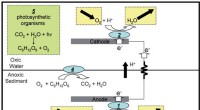 NRL udstedt patent for solar mikrobiel brændselscelleSkematisk skildring af forenklet mekanisme til energiproduktion af den bentiske mikrobielle brændselscelle (BMFC), uden boks mærket 5 svarende til fotosyntese, og for den mikrobielle fotoelektrokemisk
NRL udstedt patent for solar mikrobiel brændselscelleSkematisk skildring af forenklet mekanisme til energiproduktion af den bentiske mikrobielle brændselscelle (BMFC), uden boks mærket 5 svarende til fotosyntese, og for den mikrobielle fotoelektrokemisk
- Kopiere eller forny dig? Undersøgelse kaster lys over chimpansekulturen
- 5 Tekniske innovationer i krigen mod terrorisme
- Nyt forskningsområde:Hvordan proteinstrukturer ændrer sig på grund af normale kræfter
- Forbrugerrapporter finder, at redesign af køretøjer kommer med fejl
- Hvad er enhederne til magt?
- Hvad er nogle egenskaber eller myrer?


