Hvordan arrangerer brom sig selv som et molekyle?
Her er grunden til, at brom danner et diatomisk molekyle:
* Elektronegativitet: Bromin har en relativt høj elektronegativitet, hvilket betyder, at den stærkt tiltrækker elektroner.
* octet regel: For at opnå en stabil elektronkonfiguration skal hvert bromatom få et elektron for at afslutte sin ydre skal.
* kovalent binding: De to bromatomer deler en elektron hver og danner en enkelt kovalent binding. Denne deling giver begge atomer mulighed for at opnå en fuld oktet af elektroner.
Denne diatomiske natur er grunden til, at brom eksisterer som en rødbrun væske ved stuetemperatur, med BR 2 Molekyler holdt sammen af svage intermolekylære kræfter.
Sidste artikelHvorfor har du brug for to natriumioner for hver sulfidion i sulfid?
Næste artikelHvad er Mepiquat -chlorid?
 Varme artikler
Varme artikler
-
 Forskning afslører, hvorfor det er svært at få lugten ud af polyesterKredit:Unsplash/CC0 Public Domain Hvorfor er den yndlingsskjorte den du har båret rundt i huset siden COVID-19 startede, stadig stinker, selv efter almindelig vask? Sandsynligvis indeholder det p
Forskning afslører, hvorfor det er svært at få lugten ud af polyesterKredit:Unsplash/CC0 Public Domain Hvorfor er den yndlingsskjorte den du har båret rundt i huset siden COVID-19 startede, stadig stinker, selv efter almindelig vask? Sandsynligvis indeholder det p -
 Gecko -adhæsionsteknologi bevæger sig tættere på industrielle anvendelserEn undersøgelse ved Georgia Institute of Technology undersøgte egenskaber ved gekkoadhæsionsteknologi. Kredit:Rob Felt, Georgia Tech En gekko, der springer op ad en væg eller på tværs af et loft,
Gecko -adhæsionsteknologi bevæger sig tættere på industrielle anvendelserEn undersøgelse ved Georgia Institute of Technology undersøgte egenskaber ved gekkoadhæsionsteknologi. Kredit:Rob Felt, Georgia Tech En gekko, der springer op ad en væg eller på tværs af et loft, -
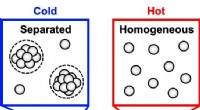 Ny model beskriver faseseparation, der ødelægger antistofopløsningerEn ny undersøgelse brugte en temperaturgradient til at observere, hvor stærkt koncentrerede antistofopløsninger, som dem, der er almindelige i nogle lægemidler, opdelt i faser, som en olie- og vandopl
Ny model beskriver faseseparation, der ødelægger antistofopløsningerEn ny undersøgelse brugte en temperaturgradient til at observere, hvor stærkt koncentrerede antistofopløsninger, som dem, der er almindelige i nogle lægemidler, opdelt i faser, som en olie- og vandopl -
 Bakteriefabrikker bruges til at opdage potentielle nye malariamedicinDerivater af violacein. Kredit:Hung-En Lai Forskere har konstrueret bakterier til at producere nye versioner af et potentielt antibiotisk molekyle, nogle med kraftige antimalariaegenskaber. Brug
Bakteriefabrikker bruges til at opdage potentielle nye malariamedicinDerivater af violacein. Kredit:Hung-En Lai Forskere har konstrueret bakterier til at producere nye versioner af et potentielt antibiotisk molekyle, nogle med kraftige antimalariaegenskaber. Brug


