Hvorfor har du brug for to natriumioner for hver sulfidion i sulfid?
* natrium (NA) er i gruppe 1 i den periodiske tabel: Dette betyder, at natriumatomer har en tendens til at miste et elektron for at blive positivt ladede ioner (Na⁺).
* svovl (er) er i gruppe 16 i den periodiske tabel: Dette betyder, at svovlatomer har en tendens til at få to elektroner til at blive negativt ladede ioner (s²⁻).
For at danne en neutral forbindelse skal de positive og negative afgifter afbalancere:
* En sulfidion (s²⁻) har en ladning på -2.
* To natriumioner (2na⁺) har en ladning på +2.
Derfor er der behov for to natriumioner for at neutralisere ladningen af en sulfidion.
Dette sikrer, at den samlede ladning af forbindelsen er nul, hvilket gør den stabil.
 Varme artikler
Varme artikler
-
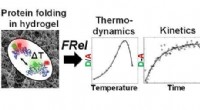 Undersøgelse af foldningsstabilitet og dynamik af proteinerForskere ved Beckman Institute ved University of Illinois brugte Fast Relaxation Imaging (FReI) til at undersøge foldningsstabiliteten og dynamikken af proteiner i polyacrylamidhydrogeler. Kredit:Ly
Undersøgelse af foldningsstabilitet og dynamik af proteinerForskere ved Beckman Institute ved University of Illinois brugte Fast Relaxation Imaging (FReI) til at undersøge foldningsstabiliteten og dynamikken af proteiner i polyacrylamidhydrogeler. Kredit:Ly -
 Feltresponsive mekaniske metamaterialer (FRMM'er)Struktur og reologiske test af MR-væske som reaktion på påførte magnetiske felter. (A) Optisk billede af MR-væsken, der danner en væskepool på et plant substrat i fravær af et magnetfelt. (B) Optisk b
Feltresponsive mekaniske metamaterialer (FRMM'er)Struktur og reologiske test af MR-væske som reaktion på påførte magnetiske felter. (A) Optisk billede af MR-væsken, der danner en væskepool på et plant substrat i fravær af et magnetfelt. (B) Optisk b -
 Molekylær lim gør perovskite solceller dramatisk mere pålidelige over tidForskere har brugt selvsamlet monolags molekylær lim til at styrke grænseflader i perovskite solceller for at gøre dem mere effektive, stabil og pålidelig. Kredit:Padture lab/Brown University Et f
Molekylær lim gør perovskite solceller dramatisk mere pålidelige over tidForskere har brugt selvsamlet monolags molekylær lim til at styrke grænseflader i perovskite solceller for at gøre dem mere effektive, stabil og pålidelig. Kredit:Padture lab/Brown University Et f -
 Udvinding af dyrebare sjældne jordarters grundstoffer fra kulflyveaske med en genanvendelig ionisk …Kredit:Grant Wilson/public domain Sjældne jordarters elementer er i mange hverdagsprodukter, såsom smartphones, LED lys og batterier. Imidlertid, kun nogle få steder har store forekomster, der er
Udvinding af dyrebare sjældne jordarters grundstoffer fra kulflyveaske med en genanvendelig ionisk …Kredit:Grant Wilson/public domain Sjældne jordarters elementer er i mange hverdagsprodukter, såsom smartphones, LED lys og batterier. Imidlertid, kun nogle få steder har store forekomster, der er
- Er Curium en leder af elektricitet?
- Bezos lover 1 milliard dollars i et forsøg på at afværge den indiske e-handelsstorm
- Nyt værktøj kan hjælpe forskere med at identificere enzymer i mikrobiomer
- Hvad er Solare Flare?
- Hvilken type blandinger adskilles ved teknikken krystallisation?
- Hvad er de grundlæggende næringsstoffer, der kræves af menneskelig krop?


