Gasmolekyler er langt fra hinanden i laget?
Her er grunden til, at gasmolekyler er langt fra hinanden:
* høj kinetisk energi: Gasmolekyler har en masse kinetisk energi, hvilket betyder, at de konstant bevæger sig og kolliderer med hinanden. Denne bevægelse holder dem spredt.
* svage intermolekylære kræfter: Kræfterne til tiltrækning mellem gasmolekyler (som van der Waals -styrker) er meget svage. Dette giver dem mulighed for let at overvinde disse kræfter og bevæge sig frit.
* Kompressibilitet: Gasser er meget komprimerbare, hvilket betyder, at du kan presse dem ind i et mindre rum. Dette skyldes, at der er en masse tom plads mellem molekylerne.
Kortfattet: Gasmolekyler er langt fra hinanden på grund af deres høje kinetiske energi, svage intermolekylære kræfter og kompressibilitet.
Sidste artikelEr phenylacetat eller butyresyre mere polær?
Næste artikelHvor mange elektroner er der i den udvidede valens for svovldioxid?
 Varme artikler
Varme artikler
-
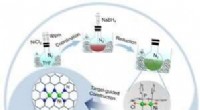 Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer
Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer -
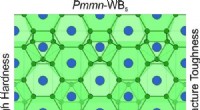 Forskere forudser et nyt superhårdt materiale med unikke egenskaberKredit:The Journal of Physical Chemistry Letters Et internationalt hold af forskere har rapporteret om et nyt superhårdt materiale, der kunne bruges til boring, maskinbygning og andre områder. D
Forskere forudser et nyt superhårdt materiale med unikke egenskaberKredit:The Journal of Physical Chemistry Letters Et internationalt hold af forskere har rapporteret om et nyt superhårdt materiale, der kunne bruges til boring, maskinbygning og andre områder. D -
 Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt
Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt -
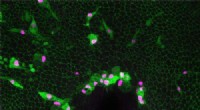 Forskere opdager kroppens beskyttelsesskjoldBillede af et fluesår og betændelse. Kredit:Helen Weavers Forskere har opdaget en måde at manipulere kroppens eget immunrespons for at øge vævsreparation. Fundene, udgivet i Aktuel biologi i dag
Forskere opdager kroppens beskyttelsesskjoldBillede af et fluesår og betændelse. Kredit:Helen Weavers Forskere har opdaget en måde at manipulere kroppens eget immunrespons for at øge vævsreparation. Fundene, udgivet i Aktuel biologi i dag
- Hvordan verden så på Huygens
- Efter at have erobret verden, smartphone går usikker fremtid i møde
- Den sidste istid fortæller os, hvorfor vi skal bekymre os om en 2-graders ændring i temperaturen
- Hvad er de mindst destruktive seismiske bølger?
- Hvilken type forvitring, der ikke ændrer mineralsammensætningen en klippe?
- Hvordan er solenergi bedre end termisk kraft?


