Hvad er den fulde elektronkonfiguration til svovl?
1S² 2S² 2P⁶ 3S² 3P⁴
Her er en sammenbrud:
* 1S²: Det første energiniveau (n =1) har et (er), der kan holde op til 2 elektroner.
* 2s²: Det andet energiniveau (n =2) har en S -sublevel, der holder 2 elektroner.
* 2p⁶: Det andet energiniveau har også et P -underniveau, der kan indeholde op til 6 elektroner.
* 3S²: Det tredje energiniveau (n =3) har en S -sublevel, der holder 2 elektroner.
* 3p⁴: Det tredje energiniveau har også et P -sublet, der har 4 elektroner til svovl.
Fortæl mig, hvis du gerne vil se orbitaldiagrammet eller den kondenserede elektronkonfiguration!
Sidste artikelDanner natriumacetat en homogen blanding i vand?
Næste artikelHvad er den molekylære formel til jern III -fluoridopløsning?
 Varme artikler
Varme artikler
-
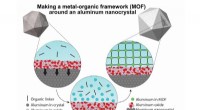 Forskere tilføjer porøs konvolut til aluminium plasmonicsEn grafik, der illustrerer syntesemetoden, der begynder med oxiddækkede aluminiumsnanokrystaller (øverst til venstre) og slutter med nanokrystallen indkapslet i metal-organisk ramme (MOF). MOFen samle
Forskere tilføjer porøs konvolut til aluminium plasmonicsEn grafik, der illustrerer syntesemetoden, der begynder med oxiddækkede aluminiumsnanokrystaller (øverst til venstre) og slutter med nanokrystallen indkapslet i metal-organisk ramme (MOF). MOFen samle -
 Smart svamp kunne rense oliespildSmart svamp absorberer selektivt olie (til venstre), mens den modstår vand (til højre). Kredit:Northwestern University Et team ledet af Northwestern University har udviklet en meget porøs smart sv
Smart svamp kunne rense oliespildSmart svamp absorberer selektivt olie (til venstre), mens den modstår vand (til højre). Kredit:Northwestern University Et team ledet af Northwestern University har udviklet en meget porøs smart sv -
 Sporing af bortskaffelse af proteiner kan føre til forbedrede behandlingerHiroaki Kiyokawa, MD, Ph.d., professor i farmakologi og patologi, var co-senior forfatter på undersøgelser publiceret i Naturkommunikation og Videnskabens fremskridt . Kredit:Northwestern Universi
Sporing af bortskaffelse af proteiner kan føre til forbedrede behandlingerHiroaki Kiyokawa, MD, Ph.d., professor i farmakologi og patologi, var co-senior forfatter på undersøgelser publiceret i Naturkommunikation og Videnskabens fremskridt . Kredit:Northwestern Universi -
 Brug af mikrobølgernes kraft til at genbruge plastKredit:mipan, Shutterstock På trods af en fortsat indsats for at reducere plastaffald, kun en brøkdel af det genbruges. For eksempel, mindre end 30 procent af plastaffaldet genbruges i EU. Noget a
Brug af mikrobølgernes kraft til at genbruge plastKredit:mipan, Shutterstock På trods af en fortsat indsats for at reducere plastaffald, kun en brøkdel af det genbruges. For eksempel, mindre end 30 procent af plastaffaldet genbruges i EU. Noget a
- Hvad sker der med bevægelsen af partikel som et stof, når dets ændringer fra fast væske?
- Hvad er den energi, der kræves for at smelte et fast stof på sit smeltepunkt?
- Hvordan den menneskelige næse Works
- Er Surface Rocky eller flad?
- Hvad er Jordens tyngdekraft i gravitationspotentiale energi?
- Undersøgelse finder en sammenhæng mellem tørke og luftkvalitet i den vestlige vildmark


