Hvad er den molekylære geometri af phosphorpentachlorid?
Her er hvorfor:
* Centralatom: Fosfor (P) er det centrale atom.
* Valenselektroner: Fosfor har 5 valenselektroner, og hvert chloratom bidrager med 1 valenselektron for i alt 10 valenselektroner.
* Elektronpar: Disse 10 elektroner danner 5 bindingspar, alle enkeltbindinger mellem fosfor og de fem kloratomer.
* Geometri: De fem bindingspar arrangerer sig i en trigonal bipyramidal form. Denne form har tre kloratomer i et trekantet plan omkring fosfor, med de to andre chloratomer placeret over og under dette plan.
Vigtig note: Den faktiske struktur af PCL5 er mere kompleks end en simpel trigonal bipyramid. Det beskrives bedre som en "forvrænget" trigonal bipyramid, hvor de aksiale P-CL-bindinger er længere end de ækvatoriale P-CL-bindinger på grund af den større frastødning mellem de aksiale kloratomer.
Sidste artikelHvad er den ædle gasnotation for Einsteinium?
Næste artikelHvorfor er ionc -forbindelser stærkere end kovalente forbindelser?
 Varme artikler
Varme artikler
-
 Ny belægning bringer lithiummetalbatteri tættere på virkelighedenHovedforfattere og ph.d. studerende David Mackanic, venstre, og Zhiao Yu med deres batteritester til højre. Yu holder et fad med allerede testede celler, som de kalder batterikirkegården. Kredit:Mark
Ny belægning bringer lithiummetalbatteri tættere på virkelighedenHovedforfattere og ph.d. studerende David Mackanic, venstre, og Zhiao Yu med deres batteritester til højre. Yu holder et fad med allerede testede celler, som de kalder batterikirkegården. Kredit:Mark -
 Iagttager en skiftende platinelektrodeKredit:Leiden University Overfladen på platinelektroder ændrer sig meget mere under brug end tidligere antaget. I et samarbejde mellem Leiden Institutes of Chemistry and Physics, kemikere Leon Jac
Iagttager en skiftende platinelektrodeKredit:Leiden University Overfladen på platinelektroder ændrer sig meget mere under brug end tidligere antaget. I et samarbejde mellem Leiden Institutes of Chemistry and Physics, kemikere Leon Jac -
 Forskere foreslår nye selektive reduktive amineringskatalysatorer med forbedret stabilitetGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c00800 Primære aminer og sekundære iminer er nøglemellemprodukter, der i vid udstrækning anvendes
Forskere foreslår nye selektive reduktive amineringskatalysatorer med forbedret stabilitetGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c00800 Primære aminer og sekundære iminer er nøglemellemprodukter, der i vid udstrækning anvendes -
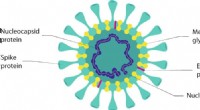 Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio
Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio
- Har NASA fundet beviser for gammelt liv Mars? En ekspert undersøger den seneste opdagelse
- Friskolers vejledning om rummelighed og klimavidenskab er baseret på evidens
- Foretager alle faste stoffer varme og samme hastighed?
- Forårsager skyer i ionosfæren regn?
- Hvordan er en stjerne i stand til at begynde heliumfusion, efter at den løb tør for brint?
- Atomenergiprogrammer øger ikke sandsynligheden for spredning, undersøgelse finder


