Hvilken slags krystallinsk fast stof er KCL?
Her er hvorfor:
* ionisk binding: KCL dannes af den elektrostatiske tiltrækning mellem positivt ladede kaliumioner (K+) og negativt ladede chloridioner (Cl-). Denne stærke elektrostatiske attraktion er det definerende egenskab ved ionisk binding.
* Krystallinsk struktur: Ioniske faste stoffer har et meget ordnet, gentagne arrangement af ioner i et tredimensionelt gitter. Dette arrangement minimerer de frastødende kræfter og maksimerer de attraktive kræfter mellem ionerne. KCL har specifikt en ansigt-centreret kubisk (FCC) krystalstruktur.
* egenskaber: Ioniske faste stoffer udviser typisk:
* Høje smeltepunkter og kogepunkter på grund af de stærke elektrostatiske kræfter.
* God elektrisk ledningsevne, når den opløses i vand eller smeltet (fordi ionerne er frie til at bevæge sig).
* Britthed på grund af den stive struktur.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelFremstilling af vask soda ved ammoniakopløsningsprocessen?
Næste artikelHvilken gas dannes, når svovl brænder?
 Varme artikler
Varme artikler
-
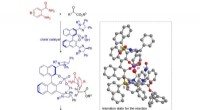 Ny metode til asymmetrisk N, N-acetalsyntese lover fremskridt inden for lægemiddeludviklingKredit:Nagoya Institute of Technology Mange af vores lægemidler og andre bioaktive lægemidler er baseret på kemiske strukturer kaldet enantiomerer - molekyler, der er spejlbilleder af hinanden og
Ny metode til asymmetrisk N, N-acetalsyntese lover fremskridt inden for lægemiddeludviklingKredit:Nagoya Institute of Technology Mange af vores lægemidler og andre bioaktive lægemidler er baseret på kemiske strukturer kaldet enantiomerer - molekyler, der er spejlbilleder af hinanden og -
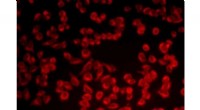 Kemikere udvikler et nyt Washington Red-farvestof til bio-billeddannelseVisualisering af cellulært svovlbrinte ved hjælp af en Washington Red-baseret fluorescerende sensor. Kredit:WSU Forskere fra Washington State University har skabt et injicerbart farvestof, der bel
Kemikere udvikler et nyt Washington Red-farvestof til bio-billeddannelseVisualisering af cellulært svovlbrinte ved hjælp af en Washington Red-baseret fluorescerende sensor. Kredit:WSU Forskere fra Washington State University har skabt et injicerbart farvestof, der bel -
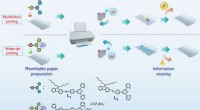 Specialpapir kan slettes og udskrives på flere gangeSkematisk illustration af flerfarve- og vandtryk. Kemiske strukturer af L 1 , L2 og L3, og udskrivnings- og sletteprocesserne for det konstruerede genskrivbare papir. Kredit: Naturkommunikation (2017
Specialpapir kan slettes og udskrives på flere gangeSkematisk illustration af flerfarve- og vandtryk. Kemiske strukturer af L 1 , L2 og L3, og udskrivnings- og sletteprocesserne for det konstruerede genskrivbare papir. Kredit: Naturkommunikation (2017 -
 Kemikere skaber en sensor, der nøjagtigt registrerer spyt-pH hos menneskerEn prøve af en kemosensor. Kredit:UrFU / Regina Pidgaetskaya Kemikere ved Ural Federal University har skabt en sensor til bestemmelse af pH i menneskeligt spyt. Dette er en fluorofor med stærk og s
Kemikere skaber en sensor, der nøjagtigt registrerer spyt-pH hos menneskerEn prøve af en kemosensor. Kredit:UrFU / Regina Pidgaetskaya Kemikere ved Ural Federal University har skabt en sensor til bestemmelse af pH i menneskeligt spyt. Dette er en fluorofor med stærk og s
- Er den følgende sætning sand eller falsk, når partikler af et objekt bevæger sig hurtigere, dens…
- Hvad er rækkefølgen af begivenhedernes rækkefølge i befrugtningen af et æg?
- Gå under jorden i Slovenien ... for at forberede sig til det ydre rum
- Hvad betyder kollisioner i gas?
- Hvordan er parasitter i stand til at genkende deres værter?
- Går Leo og Skorpionen sammen?


