Hvad er produktet, når der opstår reaktion mellem vand og kulstof?
under normale forhold (stuetemperatur og tryk):
* Ingen reaktion: Carbon er ganske inert ved stuetemperatur. Det reagerer ikke med vand for at danne nye produkter.
Under ekstreme forhold:
* Høj temperatur og tryk: Når det opvarmes til meget høje temperaturer og under tryk, kan carbon reagere med vand i en proces kaldet vandgasskiftreaktionen . Dette producerer en blanding af:
* carbonmonoxid (CO): En brandfarlig og giftig gas
* brintgas (H₂): En brandfarlig og farveløs gas
* en lille mængde kuldioxid (co₂): En farveløs og lugtfri gas
Den kemiske ligning:
C + H₂O ⇌ CO + H₂
Nøglepunkter:
* Denne reaktion er reversibel, hvilket betyder, at produkterne kan reagere tilbage på dannelse af kulstof og vand.
* Vandgasskiftreaktionen er en vigtig industriel proces til produktion af brintgas.
* Bemærk: Denne reaktion er meget eksoterm, hvilket betyder, at den frigiver en betydelig mængde varme.
Andre potentielle reaktioner:
* med damp: Når carbon reagerer med damp (vanddamp) ved høje temperaturer, producerer den carbonmonoxid og hydrogen . Dette svarer til vandgasskiftreaktionen, men involverer damp i stedet for flydende vand.
* med superkritisk vand: Under ekstreme forhold (over det kritiske vandpunkt) kan kulstof reagere med superkritisk vand for at danne forskellige produkter, herunder kuldioxid og methan .
Kortfattet:
Reaktionen mellem kulstof og vand er ikke ligetil. Resultatet afhænger stort set af temperatur- og trykforholdene. Under normale forhold forekommer der ingen reaktion. Under ekstreme forhold finder vand-gasskiftreaktionen sted, hvilket producerer kulilte, brint og kuldioxid.
Sidste artikelHvad er de kemiske egenskaber ved gruppe 8 -elementer?
Næste artikelHvilken polymer indeholder nitrogen?
 Varme artikler
Varme artikler
-
 Ny tilgang forbedrer evnen til at forudsige metals reaktioner med vandVanddråbe. Billede:Wikimedia Commons Den brede rækkevidde af korrosion, et globalt problem på flere milliarder dollars, kan en dag blive indsnævret betydeligt takket være en ny, bedre tilgang til
Ny tilgang forbedrer evnen til at forudsige metals reaktioner med vandVanddråbe. Billede:Wikimedia Commons Den brede rækkevidde af korrosion, et globalt problem på flere milliarder dollars, kan en dag blive indsnævret betydeligt takket være en ny, bedre tilgang til -
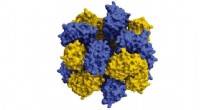 Supercomputere hjælper med at samle proteinerVed hjælp af supercomputere, forskere er lige begyndt at designe proteiner, der samler sig for at kombinere og ligne livgivende molekyler som hæmoglobin. Kredit:Taylor et al. Røde blodlegemer er f
Supercomputere hjælper med at samle proteinerVed hjælp af supercomputere, forskere er lige begyndt at designe proteiner, der samler sig for at kombinere og ligne livgivende molekyler som hæmoglobin. Kredit:Taylor et al. Røde blodlegemer er f -
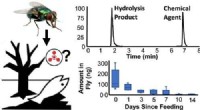 Blowfluer kan bruges til at opdage brug af kemiske våben, andre forurenende stofferGrafisk abstrakt. Miljø. Sci. Teknol. (2022). https://doi.org/10.1021/acs.est.1c07381 Forskere ved School of Science ved IUPUI har fundet ud af, at spyfluer kan bruges som kemiske sensorer, med sær
Blowfluer kan bruges til at opdage brug af kemiske våben, andre forurenende stofferGrafisk abstrakt. Miljø. Sci. Teknol. (2022). https://doi.org/10.1021/acs.est.1c07381 Forskere ved School of Science ved IUPUI har fundet ud af, at spyfluer kan bruges som kemiske sensorer, med sær -
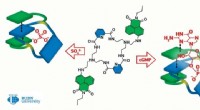 Kemikere skaber et molekyle, der kan hjælpe med at behandle hjertesygdomme og opdage viraKredit:RUDN Universitet RUDN University kemikere sammen med kolleger fra Chemnitz University of Technology (Tyskland) har syntetiseret den første kemiske receptor, der effektivt kan binde til cykl
Kemikere skaber et molekyle, der kan hjælpe med at behandle hjertesygdomme og opdage viraKredit:RUDN Universitet RUDN University kemikere sammen med kolleger fra Chemnitz University of Technology (Tyskland) har syntetiseret den første kemiske receptor, der effektivt kan binde til cykl
- Forstærkeren er den grundlæggende enhed for elektrisk?
- Forskere opdager, hvad en pansret dinosaur spiste til sit sidste måltid
- Første musikfestival går over til blockchain
- Hvad er Ernest Rutherfords bidrag til videnskab?
- Hvad sker der med massen af magnesium, når de opvarmes?
- Dræber zoom-møder kreativiteten?


