Element X findes som et ikke-polært molekyle lavet af to identiske atomer, når individuelt element reagerer med natrium, de danner ioner 2- Oplad, hvilken gruppe hører til?
* ikke -polært molekyle med to identiske atomer: Dette antyder et diatomisk molekyle, som H₂ (brint), N₂ (nitrogen), O₂ (ilt), F₂ (fluor), Cl₂ (chlor), Br₂ (brom) eller I₂ (iod).
* Formularer ioner med en 2- ladning, når man reagerer med natrium: Dette betyder, at Element X får to elektroner for at opnå en stabil oktetkonfiguration.
Bestemmelse af gruppen:
Elementer, der får to elektroner for at opnå en stabil oktet findes i gruppe 16 (via) af den periodiske tabel. Denne gruppe er også kendt som chalcogens .
Eksempel:
Oxygen (O) er et godt eksempel. Det danner et diatomisk molekyle (O₂) og reagerer med natrium for at danne natriumoxid (Na₂o), hvor ilt har en 2-ladning.
Derfor hører element X til gruppe 16 (via) i den periodiske tabel.
 Varme artikler
Varme artikler
-
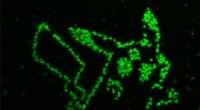 Måling af metabolitter i alger én celle ad gangenFotoporationen af en fluorogen aptamer i enkelte mikroalgeceller viser præcis, hvor den ønskede metabolit er placeret. Kredit:Yoichiroh Hosokawa I jagten på nye kilder til forbrugsvarer, vidensk
Måling af metabolitter i alger én celle ad gangenFotoporationen af en fluorogen aptamer i enkelte mikroalgeceller viser præcis, hvor den ønskede metabolit er placeret. Kredit:Yoichiroh Hosokawa I jagten på nye kilder til forbrugsvarer, vidensk -
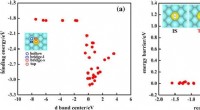 AI ledte efter enkeltatom-legeringskatalysatorer, fundet 200 lovende kandidaterFig. 1:Korrelation mellem simple deskriptorer og målegenskaber. Skoltech-forskere og deres kolleger fra Kina og Tyskland har præsenteret en ny søgealgoritme efter single-atom-legeringskatalysatore
AI ledte efter enkeltatom-legeringskatalysatorer, fundet 200 lovende kandidaterFig. 1:Korrelation mellem simple deskriptorer og målegenskaber. Skoltech-forskere og deres kolleger fra Kina og Tyskland har præsenteret en ny søgealgoritme efter single-atom-legeringskatalysatore -
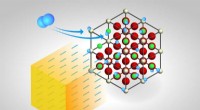 Neutronspektroskopi afslører, at almindelig iltsvampkatalysator også opsuger brintNeutroner undersøgte to mekanismer, der blev foreslået for at forklare, hvad der sker, når brintgas strømmer over en ceriumoxid (CeO2) katalysator, der er blevet opvarmet i et forsøgskammer til forske
Neutronspektroskopi afslører, at almindelig iltsvampkatalysator også opsuger brintNeutroner undersøgte to mekanismer, der blev foreslået for at forklare, hvad der sker, når brintgas strømmer over en ceriumoxid (CeO2) katalysator, der er blevet opvarmet i et forsøgskammer til forske -
 Dativ epitaksi:En ny måde at stable krystalfilm påEt scannende transmissionselektronmikroskopbillede afslører et smukt periodisk mønster (kaldet et moiré-mønster), der stammer fra det epitaksiale chromtellurid/wolframdiselenid-supergitter; overlejret
Dativ epitaksi:En ny måde at stable krystalfilm påEt scannende transmissionselektronmikroskopbillede afslører et smukt periodisk mønster (kaldet et moiré-mønster), der stammer fra det epitaksiale chromtellurid/wolframdiselenid-supergitter; overlejret


