Hvad er reaktionsvarmen for NH3 HCI --- NH4CL?
Her er hvorfor:
* eksotermisk reaktion: Reaktionen mellem ammoniak og saltsyre er en syre-base-reaktion, der danner et salt og vand. Denne type reaktion frigiver typisk varme.
* entalpiændring: Det negative tegn på reaktionsvarmen (-176,2 kJ/mol) indikerer, at reaktionen frigiver varme, hvilket gør den eksoterm.
Vigtige noter:
* Standardbetingelser: Denne værdi måles typisk under standardbetingelser (298 K og 1 ATM -tryk).
* dannelsesvarme: Reaktionsvarmen kan også beregnes ved hjælp af standardvarme af dannelse af reaktanter og produkter:
* ΔH ° (reaktion) =σ ΔH ° F (produkter) - σ ΔH ° F (reaktanter)
Fortæl mig, hvis du gerne vil udforske beregningen mere detaljeret!
Sidste artikelHvad er den nettoioniske ligning for reaktion mellem Na2SO4 og CaCl2?
Næste artikelHvordan opbevares metalnatrium?
 Varme artikler
Varme artikler
-
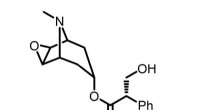 Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddelSwRI udvikler omkostningseffektive metoder til at syntetisere nye formuleringer til plantebaserede lægemidler, senest en syntetisk version af en populær behandling mod kvalme. Kredit:Southwest Researc
Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddelSwRI udvikler omkostningseffektive metoder til at syntetisere nye formuleringer til plantebaserede lægemidler, senest en syntetisk version af en populær behandling mod kvalme. Kredit:Southwest Researc -
 Består syretesten:Nyt lav-pH-system genbruger mere kulstof til værdifulde produkterPh.D. kandidat Jianan Erick Huang arbejder på en elektrolysator i laboratoriet hos professor Ted Sargent ved University of Toronto. Holdet har udviklet en ny proces til at omdanne opløst CO2 til produ
Består syretesten:Nyt lav-pH-system genbruger mere kulstof til værdifulde produkterPh.D. kandidat Jianan Erick Huang arbejder på en elektrolysator i laboratoriet hos professor Ted Sargent ved University of Toronto. Holdet har udviklet en ny proces til at omdanne opløst CO2 til produ -
 Strækbart, nedbrydelige halvledereEn ny strækbar halvleder, illustreret her, består af syrededbrydelige halvlederfibre (grønne) indlejret i en gummiagtig, bionedbrydeligt polymer. Kredit:Tilpasset fra ACS Central Science 2019, DOI:1
Strækbart, nedbrydelige halvledereEn ny strækbar halvleder, illustreret her, består af syrededbrydelige halvlederfibre (grønne) indlejret i en gummiagtig, bionedbrydeligt polymer. Kredit:Tilpasset fra ACS Central Science 2019, DOI:1 -
 Anti-degranulering og galdesyrebindende aktivitet af frugter og agroindustrielle biprodukterKredit:Anna Langova/Public Domain De ubrugte dele af frugt og grøntsager, såsom frugtkød efter juicening, indeholder ofte flere fytokemikalier med bioregulerende funktioner end de brugte dele, men
Anti-degranulering og galdesyrebindende aktivitet af frugter og agroindustrielle biprodukterKredit:Anna Langova/Public Domain De ubrugte dele af frugt og grøntsager, såsom frugtkød efter juicening, indeholder ofte flere fytokemikalier med bioregulerende funktioner end de brugte dele, men
- Tavse arter står over for udryddelse:Undersøgelse fremhæver skævhed i bevaringsforskning
- Forbrugerne nærmer sig nanopartikler
- Hvilken enhed bruges til at mærke flydende volumen?
- Hvad er strukturen af skifer, der siges at være, fordi mineralpartikler kun kan set med et mikros…
- Hvad kan få hastighed til at ændre sig?
- Hvorfor er ligningen H2 O2 - H20 ikke afbalanceret?


