Hvad er pH for natriumnitrit?
Her er hvorfor:
* Hydrolyse: Når natriumnitrit opløses i vand, adskiller den sig til natriumioner (Na⁺) og nitritioner (NO₂) ⁻. Nitritionerne reagerer med vandmolekyler for at danne nitrosyre (HNO₂) og hydroxidioner (OH⁻).
* Basisdannelse: Hydroxidionerne producerede øger pH -værdien af opløsningen, hvilket gør det grundlæggende.
Den nøjagtige pH for en natriumnitritopløsning afhænger af dens koncentration. Højere koncentrationer vil resultere i en mere grundlæggende pH.
Det er dog vigtigt at bemærke, at:
* natriumnitrit er et giftigt stof og bør håndteres med omhu.
* PH af natriumnitritopløsninger kan beregnes ved hjælp af passende kemiske ligninger og ligevægtskonstanter.
For at bestemme den nøjagtige pH for en specifik natriumnitritopløsning skal du kende dens koncentration og bruge de relevante kemiske ligevægtsudtryk.
Sidste artikelHvor mange ioner til stede i KCL?
Næste artikelHvad er en almindelig type alkan lavet tre bundne carbonatomer?
 Varme artikler
Varme artikler
-
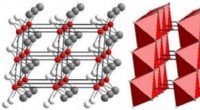 Mineralopdagelse gjort nemmere:Røntgenteknik kaster nyt lys på bittesmå, sjældne krystallerDisse diagrammer viser atomkrystalstrukturen af ognitit. Til venstre, atomer i den krystallinske struktur er repræsenteret i rødt (nikkel), hvid (tellur), og grå (vismut). Til højre, en polyhedral r
Mineralopdagelse gjort nemmere:Røntgenteknik kaster nyt lys på bittesmå, sjældne krystallerDisse diagrammer viser atomkrystalstrukturen af ognitit. Til venstre, atomer i den krystallinske struktur er repræsenteret i rødt (nikkel), hvid (tellur), og grå (vismut). Til højre, en polyhedral r -
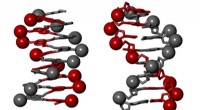 Biomimetisk kemi - DNA-mimiker overliste viralt enzymRepræsentationer af en B-DNA dobbelt helix og en enkelt spiralformet foldamer efterligner. Kredit:Ivan Huc, LMU Ikke alene kan syntetiske molekyler efterligne strukturerne i deres biologiske model
Biomimetisk kemi - DNA-mimiker overliste viralt enzymRepræsentationer af en B-DNA dobbelt helix og en enkelt spiralformet foldamer efterligner. Kredit:Ivan Huc, LMU Ikke alene kan syntetiske molekyler efterligne strukturerne i deres biologiske model -
 En mere bæredygtig måde at raffinere metaller påStrategi for at reducere miljøbelastningen af en raffineringsproces:Erstat farlige kemikalier med mere godartede og genanvendelige forbindelser. Kredit:Michael J. Krause (Western University) Et
En mere bæredygtig måde at raffinere metaller påStrategi for at reducere miljøbelastningen af en raffineringsproces:Erstat farlige kemikalier med mere godartede og genanvendelige forbindelser. Kredit:Michael J. Krause (Western University) Et -
 Fremstilling af metal-organiske ramme-baserede kompositter for effektivitetKandidatstuderende Yufeng Quan og Ruiqing Shen bruger en dobbeltskrueekstruder i bænkskala til bæredygtig og effektiv fremstilling af metal-organiske ramme-baserede polymer nanokompositter. Kredit:Dr.
Fremstilling af metal-organiske ramme-baserede kompositter for effektivitetKandidatstuderende Yufeng Quan og Ruiqing Shen bruger en dobbeltskrueekstruder i bænkskala til bæredygtig og effektiv fremstilling af metal-organiske ramme-baserede polymer nanokompositter. Kredit:Dr.
- Hvilket har den større mængde -alkoholen i et ukalibreret reagensglas eller saltopløsning et hæt…
- Forskere måler, hvor sød aftalen er for virksomheders politiske donorer
- Klar til lufttaxaer? Luftfartsingeniører og entreprenører sigter mod at ændre, hvordan vi ser him…
- Er grundfjeld lagene af sten over jord?
- Påvirker omfanget af seksuel dimorfisme i en art hastighedsudviklingen, som arter?
- Tændernes hemmelige liv:Evo-devo-modeller for tandudvikling


