Hvis opløsning A har en masse på 60 g og B 40, når de er blandet kemisk reaktion, forekommer, hvor gas produceres, hvis den endelige blanding 85, hvilken produktion?
forståelse af problemet
* massebevaring: Den samlede masse af reaktanterne (A og B) skal svare til den samlede masse af produkterne.
* Gasproduktion: Det faktum, at en gas produceres, betyder, at nogle af reaktanternes masse er blevet omdannet til en gasformig form, der slipper ud i atmosfæren.
Beregninger
1. Total reaktantmasse: 60 g (a) + 40 g (b) =100 g
2. Manglende masse: 100 g (reaktanter) - 85 g (blanding) =15 g
3. Konklusion: 15 g af reaktanterne blev omdannet til en gas, der slap væk.
Vigtig note: Vi kan ikke bestemme de nøjagtige kemiske produkter uden mere information om den specifikke reaktion mellem A og B. De manglende 15 g kunne skyldes en række forskellige gasser, der produceres.
eksempel scenarie
Lad os forestille os en hypotetisk reaktion:
* a: Natriumbicarbonat (NAHCO3) - Bagepulver
* b: Eddike (eddikesyre, ch3cooh)
Denne reaktion producerer kuldioxidgas (CO2), vand (H2O) og natriumacetat (NAC2H3O2). De 15 g manglende vil sandsynligvis skyldes, at kuldioxidgas undslipper.
for at løse dette fuldstændigt
Du har brug for mere information, såsom:
* Identiteterne af stoffer A og B: Dette er afgørende for at kende den kemiske reaktion, der opstår.
* den afbalancerede kemiske ligning: Dette viser det nøjagtige forhold mellem reaktanter og produkter.
Fortæl mig, hvis du har flere detaljer om reaktionen, og jeg kan hjælpe dig med at finde ud af de specifikke produkter!
Sidste artikelHvad er Alkanides?
Næste artikelHvor mange elektroner er der i orbitaler relateret til det 3. energiniveau af et svovlatom?
 Varme artikler
Varme artikler
-
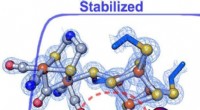 Forskere finder, hvordan enzymmiljø ændrer hastigheden og retningen af en reaktionForskere fandt ud af, at subtile ændringer i proteinstilladet omkring et enzyms katalytiske center på eksakt måde styrer hastigheden og retningen af kemiske reaktioner. Inden for [FeFe] -hydrogenase
Forskere finder, hvordan enzymmiljø ændrer hastigheden og retningen af en reaktionForskere fandt ud af, at subtile ændringer i proteinstilladet omkring et enzyms katalytiske center på eksakt måde styrer hastigheden og retningen af kemiske reaktioner. Inden for [FeFe] -hydrogenase -
 Forskere udvikler levedygtige, miljøvenligt alternativ til StyrofoamEn miljøvenlig, plantebaseret materiale, der for første gang fungerer bedre end Styrofoam til isolering. Kredit:WSU Washington State University forskere har udviklet en miljøvenlig, plantebaseret
Forskere udvikler levedygtige, miljøvenligt alternativ til StyrofoamEn miljøvenlig, plantebaseret materiale, der for første gang fungerer bedre end Styrofoam til isolering. Kredit:WSU Washington State University forskere har udviklet en miljøvenlig, plantebaseret -
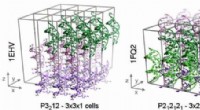 Forskere opnår de første stabile simuleringer af DNA -krystallerDe tre krystal systemer undersøgt i denne undersøgelse. Disse systemer indeholder (fra venstre mod højre) 27, Henholdsvis 24 og 36 dobbeltstrenget DNA. Kredit:Pablo Dans Puiggròs, IRB Barcelona Si
Forskere opnår de første stabile simuleringer af DNA -krystallerDe tre krystal systemer undersøgt i denne undersøgelse. Disse systemer indeholder (fra venstre mod højre) 27, Henholdsvis 24 og 36 dobbeltstrenget DNA. Kredit:Pablo Dans Puiggròs, IRB Barcelona Si -
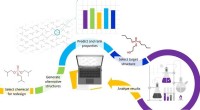 Sådan designes sikre og bæredygtige kemikalierMetode præsenteret af forskerne. Som et casestudie genererede de over seks millioner alternativer til en populær flammehæmmer og evaluerede deres egenskaber. Kredit:UvA/HIMS Med mange menneskeskabt
Sådan designes sikre og bæredygtige kemikalierMetode præsenteret af forskerne. Som et casestudie genererede de over seks millioner alternativer til en populær flammehæmmer og evaluerede deres egenskaber. Kredit:UvA/HIMS Med mange menneskeskabt
- En vellykket COP26 er afgørende for Jordens fremtid. Her er hvad der skal gå rigtigt
- Tidlig talforståelse for elever i første klasse
- Proteinkrystaller dyrket i mikrotyngdekraft kunne give modgift mod nervestoffer
- Beskyttelse mod digitale guldgravere – software blokerer kryptomining
- Næste generation af fotodetektorkamera, der skal implementeres under demonstrationsmission for robo…
- Hvordan opdele Square Feet


