Hvad er den afbalancerede ligning, når jod reagerer med natriumhydroxid?
3 i₂ (s) + 6 NaOH (aq) → 5 NAI (aq) + naio₃ (aq) + 3 h₂o (l)
Forklaring:
* reaktanter: Jod (I₂) er et fast, og natriumhydroxid (NaOH) er en vandig opløsning.
* Produkter:
* Natriumiodid (NAI) dannes som et resultat af reduktionen af jod.
* Natriumiodat (naio₃) dannes som et resultat af oxidation af jod.
* Vand (H₂O) produceres også.
Sådan fungerer reaktionen:
1. uforholdsmæssig: Jod (i₂) er både oxideret og reduceret.
* Oxidation: Nogle jodatomer mister elektroner og bliver iodationer (IO₃⁻).
* reduktion: Andre jodatomer får elektroner og bliver iodidioner (I⁻).
2. reaktion med NaOH: Iodidionerne reagerer med natriumhydroxid for at danne natriumiodid (NAI) og vand. Iodaterne reagerer også med natriumhydroxid for at danne natriumiodat (naio₃) og vand.
Vigtige noter:
* Reaktionen udføres normalt i en varm løsning for at fremskynde processen.
* Reaktionen producerer en gul opløsning på grund af dannelsen af triiodidioner (I₃⁻).
* Denne reaktion bruges ofte til at fremstille natriumiodat, der bruges i forskellige anvendelser, herunder som et reagens i analytisk kemi.
 Varme artikler
Varme artikler
-
 Fremme i forståelsen af all-solid-state batterierSkematisk af Li-metal/Li6PS5Cl-grænsefladen cyklet ved en samlet strømtæthed over CCS. Kredit: Naturmaterialer (2019) All-solid-state batterier, et batteridesign bestående af alle solide komponen
Fremme i forståelsen af all-solid-state batterierSkematisk af Li-metal/Li6PS5Cl-grænsefladen cyklet ved en samlet strømtæthed over CCS. Kredit: Naturmaterialer (2019) All-solid-state batterier, et batteridesign bestående af alle solide komponen -
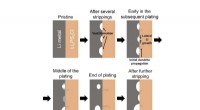
 En ny måde at kombinere bløde materialer påEn umodificeret hydrogel (til venstre) skræller let af fra en elastomer. En kemisk bundet hydrogel og elastomer (til højre) er svære at skille fra hinanden, efterlader rester efter kredit:Suo Lab/Harv
En ny måde at kombinere bløde materialer påEn umodificeret hydrogel (til venstre) skræller let af fra en elastomer. En kemisk bundet hydrogel og elastomer (til højre) er svære at skille fra hinanden, efterlader rester efter kredit:Suo Lab/Harv -
 Fremtiden for plastik – genbruge det dårlige og opmuntre det godePlastforurening:kasserede plastikposer er en fare for livet i havet. Kredit:Richard Whitcombe/Shutterstock, CC BY-ND Plast har fået et dårligt navn, hovedsagelig af to grunde:de fleste er lavet af
Fremtiden for plastik – genbruge det dårlige og opmuntre det godePlastforurening:kasserede plastikposer er en fare for livet i havet. Kredit:Richard Whitcombe/Shutterstock, CC BY-ND Plast har fået et dårligt navn, hovedsagelig af to grunde:de fleste er lavet af -
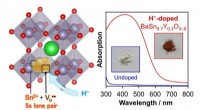 Vellykket syntese af perovskit synligt lysabsorberende halvledermaterialeEt billigere perovskit-baseret halvledermateriale, der er fri for giftigt bly og kan absorbere en bred vifte af synligt lys med potentielle fotofunktionelle applikationer. Kredit:Materialekemi Hal
Vellykket syntese af perovskit synligt lysabsorberende halvledermaterialeEt billigere perovskit-baseret halvledermateriale, der er fri for giftigt bly og kan absorbere en bred vifte af synligt lys med potentielle fotofunktionelle applikationer. Kredit:Materialekemi Hal
- Hvad er en type fossil, der ikke er en organisme?
- Coronavirus-pandemien kræver, at vi forstår fødevarers uklare forsyningskæder
- Hvad er kilden til mineralmateriale, der findes i jord?
- Er Mælkevejen en 'outlier' galakse? Studerer sine 'søskende' for spor
- Hvordan påvirker tiden pH i appelsinsaft?
- Frø af verdens sjældneste træer og afgrøder kan ikke bankes


