Bindingerne inden for polyatomiske ioner er overvejende?
Her er hvorfor:
* kovalente obligationer Involver deling af elektroner mellem atomer. Polyatomiske ioner består af flere atomer, der holdes sammen ved deling af elektroner.
* ioniske bindinger Involver overførsel af elektroner fra et atom til et andet, danner ioner med modsatte ladninger, der tiltrækker hinanden. Mens polyatomiske ioner har en samlet ladning, holdes de individuelle atomer inden for ion sammen af delte elektroner, ikke en komplet overførsel.
Eksempel:
Sulfationen (SO₄²⁻) er en polyatomisk ion. Svovlatomet deler elektroner med de fire iltatomer og danner kovalente bindinger. Den samlede ladning på -2 er fordelt over hele ionen.
Kortfattet: Polyatomiske ioner holdes sammen ved deling af elektroner, der er karakteristisk for kovalente bindinger.
 Varme artikler
Varme artikler
-
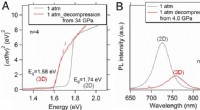 Trykinduceret 2D-3D konvertering i hybrid blyiodid lagdelt perovskit2D-3D overgang i hybrid perovskites. Kredit:Gang Liu Hydrostatisk tryk kan føre til nye og forbedrede materialeegenskaber. Imidlertid, de fleste nye materialeegenskaber kan kun bevares ved højtryk
Trykinduceret 2D-3D konvertering i hybrid blyiodid lagdelt perovskit2D-3D overgang i hybrid perovskites. Kredit:Gang Liu Hydrostatisk tryk kan føre til nye og forbedrede materialeegenskaber. Imidlertid, de fleste nye materialeegenskaber kan kun bevares ved højtryk -
 Guldbindingsdannelse spores i realtid ved hjælp af ny molekylær spektroskopi-teknikFigur 1:Et formskiftende molekyle snapper fra en bøjet (øverst til højre) til en lige struktur (nederst til højre), når det rammes af en ultraviolet laserimpuls (lilla krumspring øverst i midten). To
Guldbindingsdannelse spores i realtid ved hjælp af ny molekylær spektroskopi-teknikFigur 1:Et formskiftende molekyle snapper fra en bøjet (øverst til højre) til en lige struktur (nederst til højre), når det rammes af en ultraviolet laserimpuls (lilla krumspring øverst i midten). To -
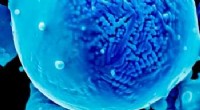 Tilpasning af legeringens mikrokemi til fejlfri metal 3D -printEn ny metode udviklet af Texas A&M-forskere optimerer legeringsegenskaber og procesparametre til at skabe overlegne 3D-printede metaldele. Her er vist et farvet elektronmikrograf af en nikkelpulverleg
Tilpasning af legeringens mikrokemi til fejlfri metal 3D -printEn ny metode udviklet af Texas A&M-forskere optimerer legeringsegenskaber og procesparametre til at skabe overlegne 3D-printede metaldele. Her er vist et farvet elektronmikrograf af en nikkelpulverleg -
 Video:Olivenolies kemiKredit:The American Chemical Society Uanset om du suger det op med brød eller bruger det til at booste din madlavning, olivenolie er fantastisk. Men der foregår en masse kemi i den flaske, der ka
Video:Olivenolies kemiKredit:The American Chemical Society Uanset om du suger det op med brød eller bruger det til at booste din madlavning, olivenolie er fantastisk. Men der foregår en masse kemi i den flaske, der ka
- Ny model hjælper med at definere optimal temperatur og tryk for at smede nanoskala diamanter
- Vil en kugle lande i samme hastighed som kuglen, hvis du falder eller skyder den tid og højde?
- Hvilken klippe er almindeligt sammensat af de rester dyre skaller?
- Resultater på A-niveau viser de mønstre af ulemper, regeringen skal tackle
- Isolering af intakte bakterier fra blod ved hjælp af en mikrofluidisk monolitanordning
- Hvor lang revolution af Saturn?


