Hvad billed rutherford te atom som?
* kernen: Han så for sig en lille, tæt, positivt ladet kerne i midten af atomet, ligesom solen i vores solsystem.
* Elektroner: Han tænkte på elektroner, negativt ladede partikler, der kredse kernen, som planeter, der kredser om solen.
* tomt rum: Det meste af atomet var ifølge Rutherford tom plads, ligesom rummet mellem planeter i vores solsystem.
Denne model var et revolutionerende skridt fremad fra den tidligere "blomme budding" -model, der forestillede sig en positivt ladet sfære med elektroner indlejret i den. Rutherfords model forklarede resultaterne af hans guldfolieeksperiment, som viste, at de fleste alfapartikler passerede lige gennem folien, mens nogle få blev afbøjet i store vinkler, hvilket antydede en koncentreret positiv ladning i centrum.
Det er vigtigt at huske, at Rutherfords model senere blev forfinet af Niels Bohr og andre, hvilket førte til den kvantemekaniske model for atomet, som vi forstår i dag. Imidlertid gav Rutherfords solsystemmodel et afgørende fundament for vores forståelse af atomstruktur.
Sidste artikelHvad er egenskaberne ved radioaktive partikler?
Næste artikelHvad findes partiklerne i kernen i alle atomer?
 Varme artikler
Varme artikler
-
 Geler lavet af dråber er mindre stabile end geler lavet af faste partiklerSynereseforskning om tiltrækning mellem dråber og partikler i væskelag af WUR Geler lavet af dråber er mindre stabile end geler lavet af faste partikler. Som resultat, dråber udviser også meget hu
Geler lavet af dråber er mindre stabile end geler lavet af faste partiklerSynereseforskning om tiltrækning mellem dråber og partikler i væskelag af WUR Geler lavet af dråber er mindre stabile end geler lavet af faste partikler. Som resultat, dråber udviser også meget hu -
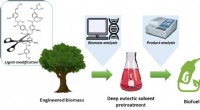 Team udvikler biobrændstofproduktionsproces i samarbejde med nordamerikanske forskereForskerne var i stand til at maksimere og kombinere potentialet i flere forskellige områder for produktion af biobrændstoffer, herunder genteknologi, procesteknologi, og analyseteknologi. Kredit:Korea
Team udvikler biobrændstofproduktionsproces i samarbejde med nordamerikanske forskereForskerne var i stand til at maksimere og kombinere potentialet i flere forskellige områder for produktion af biobrændstoffer, herunder genteknologi, procesteknologi, og analyseteknologi. Kredit:Korea -
 Forskere forbinder kvartsmikrobalancemålinger med internationalt målesystemModsatte sider af en kvartskrystalresonator. Kredit:Bæger via Wikipedia Forskere ved National Institute of Standards and Technology (NIST) har fundet en måde at forbinde målinger foretaget af en e
Forskere forbinder kvartsmikrobalancemålinger med internationalt målesystemModsatte sider af en kvartskrystalresonator. Kredit:Bæger via Wikipedia Forskere ved National Institute of Standards and Technology (NIST) har fundet en måde at forbinde målinger foretaget af en e -
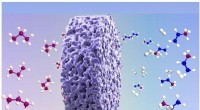 Centimeter-skala porøse enkeltkrystallinske monolitter med Lewis-syresider med høj densitet for at…Centimeterskala mesoporøse enkeltkrystaller monolitter med høj-densitet Lewis-syre-steder på snoet overflade og klart aktive steder leverer forbedret propan-dehydrogenering ved reduceret temperatur. K
Centimeter-skala porøse enkeltkrystallinske monolitter med Lewis-syresider med høj densitet for at…Centimeterskala mesoporøse enkeltkrystaller monolitter med høj-densitet Lewis-syre-steder på snoet overflade og klart aktive steder leverer forbedret propan-dehydrogenering ved reduceret temperatur. K
- Forskere afslører nye spor i, hvordan Jorden fik sin ilt
- Hvordan ville en skabning se ud som at leve på Saturn planeten?
- Hvad er den kemiske ændring, når et lys lyser?
- Hvordan ændres tyngdekraften mellem to kroppe, når afstand dem øges med 4?
- Forskere vender scriptet om magnetocapacitance
- Hvilke typer blødt trætræer vokser i regnskoven?


