Hvorfor faste stoffer vil have mindre energi end de samme materialer i flydende eller gastilstand?
* Energi og molekylær bevægelse: Energien fra et stof er direkte relateret til bevægelsen af dets molekyler. Jo mere molekylerne bevæger sig og vibrerer, jo højere er energien.
* Stater af stof:
* faste stoffer: Molekyler i faste stoffer er tæt pakket og har begrænset bevægelse. De vibrerer i faste positioner.
* væsker: Molekyler i væsker har mere frihed til at bevæge sig rundt i hinanden. De kan oversætte, rotere og vibrere, hvilket resulterer i mere energi.
* Gasser: Molekyler i gasser har mest frihed. De bevæger sig hurtigt i alle retninger, kolliderer med hinanden og er langt fra hinanden. Dette giver gasser de højeste energiniveau.
Her er en analogi: Forestil dig en flok mennesker i en overfyldt elevator (solid). De kan næppe bevæge sig. Forestil dig dem nu i et overfyldt tog (væske). De kan bevæge sig rundt, men deres bevægelser er stadig begrænset. Endelig forestil dig dem i et stort åbent felt (gas). De kan bevæge sig frit og løbe i alle retninger.
Kortfattet:
* faste stoffer har mindst energi, fordi deres molekyler har mindst bevægelse.
* væsker har mere energi end faste stoffer, fordi deres molekyler har mere bevægelsesfrihed.
* Gasser har mest energi, fordi deres molekyler bevæger sig mest frit.
Derfor tager det energi at smelte et fast stof til en væske eller for at fordampe en væske til en gas. Du tilføjer energi til molekylerne, øger deres bevægelse og ændrer deres tilstand.
 Varme artikler
Varme artikler
-
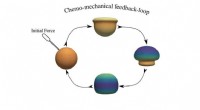 Design af bløde materialer, der efterligner biologiske funktionerKredit:Northwestern University Northwestern Engineering forskere har udviklet en teoretisk model til at designe bløde materialer, der demonstrerer autonome oscillerende egenskaber, der efterligner
Design af bløde materialer, der efterligner biologiske funktionerKredit:Northwestern University Northwestern Engineering forskere har udviklet en teoretisk model til at designe bløde materialer, der demonstrerer autonome oscillerende egenskaber, der efterligner -
 Spin-out-virksomhed hjælper med at få effektive lægemidler på markedet, hurtigere og billigereKredit:Swansea University At få bedre stoffer på markedet hurtigere, og til en brøkdel af prisen, er et skridt nærmere takket være teknologi til at fremskynde testprocessen, som udvikles af et spi
Spin-out-virksomhed hjælper med at få effektive lægemidler på markedet, hurtigere og billigereKredit:Swansea University At få bedre stoffer på markedet hurtigere, og til en brøkdel af prisen, er et skridt nærmere takket være teknologi til at fremskynde testprocessen, som udvikles af et spi -
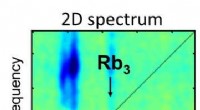 Forskere anvender 2-D spektroskopi til isolerede molekylære systemer for første gang2-D spektroskopi illustrerer de lysinducerede reaktioner af Rubidium molekyler i forskellige farvespektre. Illustration:Lukas Bruder Et forskerhold ledet af Prof. Dr. Frank Stienkemeier og Dr. Luk
Forskere anvender 2-D spektroskopi til isolerede molekylære systemer for første gang2-D spektroskopi illustrerer de lysinducerede reaktioner af Rubidium molekyler i forskellige farvespektre. Illustration:Lukas Bruder Et forskerhold ledet af Prof. Dr. Frank Stienkemeier og Dr. Luk -
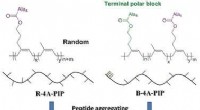 Biomimetisk strategi fører til stærke, genanvendeligt gummiKredit:Wiley Inspireret af naturen, Kinesiske videnskabsmænd har fremstillet en syntetisk analog til vulkaniseret naturgummi. Deres materiale er lige så hårdt og holdbart som originalen. I journal
Biomimetisk strategi fører til stærke, genanvendeligt gummiKredit:Wiley Inspireret af naturen, Kinesiske videnskabsmænd har fremstillet en syntetisk analog til vulkaniseret naturgummi. Deres materiale er lige så hårdt og holdbart som originalen. I journal
- Hvilke planter får du i regnskoven?
- Hvad er 35 graders i Celsius -skala?
- Find ud af navn på ting, der fungerer som dirigent og isolator?
- Californiens misforståede forsøg på at tvinge bytæthed
- Tosprogede børn kan ikke slukke for deres sprogkundskaber, siger forsker
- De fleste medarbejdere kan arbejde smartere, givet chancen


