Hvilke former dannes ikke carbonhydrider?
* De danner ikke perfekte geometriske former som terninger eller pyramider. Dette skyldes, at bindingerne mellem carbonatomer er tetrahedrale, hvilket betyder, at de danner en 3-dimensionel form med fire hjørner, ikke de lige linjer og vinkler i geometriske former.
* De danner heller ikke meget polære former. Dette skyldes, at kulstof og brint har lignende elektronegativitet, hvilket betyder, at de ikke danner stærke dipoler som vand gør.
Almindelige former for kulbrinter
* lineær: Lige kæder af carbonatomer.
* forgrenet: Kæder med carbonatomer, der forgrener hovedkæden.
* cyklisk: Ringe af carbonatomer.
* aromatisk: Cykliske strukturer med vekslende enkelt- og dobbeltobligationer.
Vigtig note: Formerne af kulbrinter er afgørende for deres egenskaber. Lineære kæder er mere fleksible, mens cykliske strukturer er mere stive. Forgrenede strukturer kan påvirke kogepunktet og opløseligheden. Aromatiske strukturer er ofte meget stabile.
 Varme artikler
Varme artikler
-
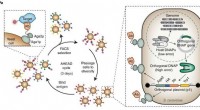 Nyt værktøj har til formål at bekæmpe COVID-19, andre sygdommeFig. 1:Autonom hypermutation gæroverfladevisning (AHEAD). en, Skema for den hurtige udvikling af højaffinitetsbinding ved hjælp af AHEAD. Ab, antistoffragment; DNAP, DNA-polymerase; HA, hæmagglutinin
Nyt værktøj har til formål at bekæmpe COVID-19, andre sygdommeFig. 1:Autonom hypermutation gæroverfladevisning (AHEAD). en, Skema for den hurtige udvikling af højaffinitetsbinding ved hjælp af AHEAD. Ab, antistoffragment; DNAP, DNA-polymerase; HA, hæmagglutinin -
 Her kommer solen:en ny ramme for kunstig fotosynteseKredit:RapidEye/iStock Forskere har længe forsøgt at efterligne den proces, hvorved planter fremstiller deres eget brændstof ved hjælp af sollys, carbondioxid, og vand gennem kunstige fotosyntesea
Her kommer solen:en ny ramme for kunstig fotosynteseKredit:RapidEye/iStock Forskere har længe forsøgt at efterligne den proces, hvorved planter fremstiller deres eget brændstof ved hjælp af sollys, carbondioxid, og vand gennem kunstige fotosyntesea -
 En naturligt inspireret, genanvendeligt system, der renser vand og bygger sig selvEt nyt materiale udviklet af forskere fra Penn State kunne en dag bruges til at fjerne vedvarende forurenende stoffer fra drikkevand. Kredit:ISTOCK/@HYRMA I naturen, interaktionen mellem molekyler
En naturligt inspireret, genanvendeligt system, der renser vand og bygger sig selvEt nyt materiale udviklet af forskere fra Penn State kunne en dag bruges til at fjerne vedvarende forurenende stoffer fra drikkevand. Kredit:ISTOCK/@HYRMA I naturen, interaktionen mellem molekyler -
 De miljømæssige omkostninger ved fast fashionIkke mere nøjes og repareres. Kredit:wwww.shutterstock.com Det er svært at elske vores tøj og blive ved med at have det på i længere tid, når vi står over for en fristende række af nyheder på tilb
De miljømæssige omkostninger ved fast fashionIkke mere nøjes og repareres. Kredit:wwww.shutterstock.com Det er svært at elske vores tøj og blive ved med at have det på i længere tid, når vi står over for en fristende række af nyheder på tilb


