Hvad er den videnskabelige forklaring på lag af væsker?
Intermolekylære kræfter:
* attraktive kræfter: Disse kræfter holder molekyler sammen. De kan kategoriseres i forskellige typer, såsom:
* Hydrogenbinding: Stærkeste type, der involverer et hydrogenatom bundet til et stærkt elektronegativt atom som ilt eller nitrogen.
* dipol-dipolinteraktioner: Forekommer mellem polære molekyler med permanente dipoler.
* London Dispersion Forces: Svageste type, der forekommer mellem alle molekyler på grund af midlertidige udsving i elektronfordeling.
* frastødende kræfter: Disse kræfter forhindrer molekyler i at komme for tæt på hinanden.
ublandbarhed:
Når to væsker er ikke -blandbare, er attraktive kræfter mellem molekylerne af den samme væske stærkere end de attraktive kræfter mellem molekylerne i de forskellige væsker. Dette betyder:
* væske A molekyler foretrækker at være omgivet af andre væske A molekyler.
* flydende B -molekyler foretrækker at være omgivet af andre flydende B -molekyler.
Dette fører til faseseparation , hvor de to væsker danner forskellige lag. tættere væske vil slå sig ned i bunden, mens mindre tæt væske vil flyde på toppen.
Eksempler:
* olie og vand: Vand er polært og danner brintbindinger, mens olie er ikke -polært og domineret af London -spredningskræfter. Disse forskelle i intermolekylære kræfter gør dem ikke blandbare.
* kviksølv og vand: Kviksølv er et tungmetal med stærke metalliske bindinger, mens vand er polært. Deres forskellige intermolekylære kræfter forhindrer dem i at blande.
Undtagelser:
Mens forskellen i intermolekylære kræfter er den primære årsag til ublandbarhed, er der nogle undtagelser. For eksempel kan nogle væsker danne emulsioner , som er stabile dispersioner af en væske i en anden. Dette kræver ofte tilstedeværelsen af en emulgator , et stof, der reducerer overfladespændingen mellem væskerne og giver dem mulighed for at blande.
Kortfattet: Dannelsen af lag i væsker skyldes forskellene i intermolekylære kræfter mellem molekylerne i de forskellige væsker. Den stærkere tiltrækning mellem molekyler af samme type fører til faseseparation og dannelsen af forskellige lag.
 Varme artikler
Varme artikler
-
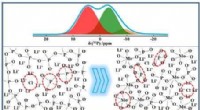 Forskere undersøger strukturen af fosfat-ionisk ledende glas ved hjælp af solid-state NMRStrukturudviklingen af hurtige ionledende glas karakteriseret ved brug af solid-state NMR-teknologier. Kredit:SIOM Glasagtige hurtige ioniske ledere kan bruges som faste elektrolytter, katode ma
Forskere undersøger strukturen af fosfat-ionisk ledende glas ved hjælp af solid-state NMRStrukturudviklingen af hurtige ionledende glas karakteriseret ved brug af solid-state NMR-teknologier. Kredit:SIOM Glasagtige hurtige ioniske ledere kan bruges som faste elektrolytter, katode ma -
 Vanedannende nødderivater kan hjælpe rygere med at bryde nikotinvanenForbindelser afledt af arecanødder kan hjælpe cigaretrygere med at holde op. Kredit:Roger Papke, Ph.d. Hele 600 millioner mennesker i Sydøstasien tygger arecanødder med betelblade, nogle gange til
Vanedannende nødderivater kan hjælpe rygere med at bryde nikotinvanenForbindelser afledt af arecanødder kan hjælpe cigaretrygere med at holde op. Kredit:Roger Papke, Ph.d. Hele 600 millioner mennesker i Sydøstasien tygger arecanødder med betelblade, nogle gange til -
 Koordineringspolymerer med op til 99,99% antibakteriel effektivitetKredit:RUDN University En kemiker ved RUDN University har sammen med sine kolleger fra Portugal udviklet to typer belægninger baseret på nye koordineringspolymerer med sølv. Begge forbindelser ble
Koordineringspolymerer med op til 99,99% antibakteriel effektivitetKredit:RUDN University En kemiker ved RUDN University har sammen med sine kolleger fra Portugal udviklet to typer belægninger baseret på nye koordineringspolymerer med sølv. Begge forbindelser ble -
 Touchscreen-alternativ dæmper frygten for verdensmangel på indiumDet nye materiale er skabt ved hjælp af en proces kaldet plasmasputtering. Kredit:Behnam Akhavan Har du nogensinde forestillet dig din smartphone eller tablet uden en berøringsskærm? Dette kan sna
Touchscreen-alternativ dæmper frygten for verdensmangel på indiumDet nye materiale er skabt ved hjælp af en proces kaldet plasmasputtering. Kredit:Behnam Akhavan Har du nogensinde forestillet dig din smartphone eller tablet uden en berøringsskærm? Dette kan sna
- Hvilken komponent reduceres under elektrolysen af saltvand?
- Hvad er enheder, der bruger elektromagneter?
- Flyvning efter den kolde krigs tidslinje
- Vores forskning viser, at børn producerer bedre stykker skrift i hånden. Men de har også brug for…
- Hvor mange overflader har jorden?
- Hvilke tre forhold studerer økologer?


