Hvorfor vendes kemisk forandring?
kemiske ændringer, der kan vendes
* reversible reaktioner: Nogle kemiske reaktioner kan fortsætte i begge retninger, hvilket betyder, at produkterne kan reagere for at danne de originale reaktanter. Dette er ofte angivet med en dobbelt pil (⇌).
* Eksempel: Dannelsen af ammoniak fra nitrogen og brint er reversibel:
N₂ + 3H₂ ⇌ 2NH₃
* Fysiske ændringer: Mange ændringer, vi tænker på som kemiske, er faktisk fysiske ændringer, der kan vendes. Disse involverer ændringer i tilstand eller form, ikke sammensætningen af stoffet.
* Eksempel: Smelteis (fast vand) i flydende vand er reversibelt ved at fryse det tilbage i is.
kemiske ændringer, der er vanskelige eller umulige at vende
* irreversible reaktioner: Nogle reaktioner er irreversible, hvilket betyder, at produkterne ikke let kan reagere på at danne de originale reaktanter. Disse involverer ofte:
* Dannelse af en gas: Brændende træ frigiver kuldioxid, som ikke let rekombineres med den resterende aske.
* Dannelse af et bundfald: Blanding af opløsninger af blynitrat og kaliumiodidformer bly iodidudfældning. Selvom det er muligt at adskille bundfaldet, er det ikke det samme som at vende den kemiske reaktion.
* Nedbrydningsreaktioner: At opdele store molekyler i mindre kan være vanskelige at vende (f.eks. Brændende brændstof).
Faktorer, der påvirker reversibilitet
* Energi: Kemiske reaktioner, der frigiver en masse energi (eksotermisk), er generelt sværere at vende end dem, der absorberer energi (endotermisk).
* entropi: Reaktioner, der øger lidelse (entropi), er vanskeligere at vende end dem, der mindsker forstyrrelsen.
* Betingelser: Temperatur, tryk og katalysatorer kan påvirke reversibiliteten af en reaktion.
Nøglepunkt: Hvorvidt en kemisk ændring kan vendes, afhænger af den involverede specifikke reaktion og betingelserne under hvilke den forekommer.
 Varme artikler
Varme artikler
-
 En biosensor registrerer forfalskning af hest i oksekød inden for en timeBiosensoren registrerer en forurening på kun 0,5 procent af hestekødet. Kredit:Nate Stelner Forfalskning af oksekød med hestekød kan nu påvises med en elektrokemisk biosensor udviklet af Compluten
En biosensor registrerer forfalskning af hest i oksekød inden for en timeBiosensoren registrerer en forurening på kun 0,5 procent af hestekødet. Kredit:Nate Stelner Forfalskning af oksekød med hestekød kan nu påvises med en elektrokemisk biosensor udviklet af Compluten -
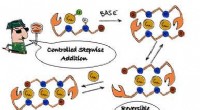 Bygning af molekylære ledninger, et atom ad gangenEn tegneserie af Dr. Rivada-Wheelaghan viser den enkle trinvise proces med kobberatomkædesyntese ved hjælp af en dynamisk ligand. Kobberatomer kan tilføjes eller fjernes en efter en for at lave kæder
Bygning af molekylære ledninger, et atom ad gangenEn tegneserie af Dr. Rivada-Wheelaghan viser den enkle trinvise proces med kobberatomkædesyntese ved hjælp af en dynamisk ligand. Kobberatomer kan tilføjes eller fjernes en efter en for at lave kæder -
 Venetiansk læge havde en central rolle i udformningen af den tidlige moderne kemiSantorios marginale note til kol. 406C-D, i Santorio Santori, Commentaria In Primam Fen Primi Libri Canonis Avicennae (Venedig, 1625), British Library, 542.h.11. Kredit:Santorios marginale note til ko
Venetiansk læge havde en central rolle i udformningen af den tidlige moderne kemiSantorios marginale note til kol. 406C-D, i Santorio Santori, Commentaria In Primam Fen Primi Libri Canonis Avicennae (Venedig, 1625), British Library, 542.h.11. Kredit:Santorios marginale note til ko -
 Kugler kan gøre beton slankere, grønnerePakket, mikronskala calciumsilikatkugler udviklet ved Rice University er et lovende materiale, der kan føre til stærkere og mere miljøvenlig beton. Kredit:Multiscale Materials Laboratory/Rice Universi
Kugler kan gøre beton slankere, grønnerePakket, mikronskala calciumsilikatkugler udviklet ved Rice University er et lovende materiale, der kan føre til stærkere og mere miljøvenlig beton. Kredit:Multiscale Materials Laboratory/Rice Universi


