Hvad er ligheden mellem partikler af væsker og faste stoffer?
Her er en sammenbrud:
væsker:
* Partikler er tæt pakket Men har mere bevægelsesfrihed end faste stoffer.
* De kan glide forbi hinanden og tag formen på deres beholder.
* Intermolekylære kræfter er svagere end i faste stoffer, der giver mulighed for denne bevægelse.
faste stoffer:
* Partikler er tæt pakket og tæt bundet i et fast arrangement.
* De vibrerer på plads Og kan ikke glide forbi hinanden .
* Intermolekylære kræfter er stærkere end i væsker, hvilket giver faste stoffer deres stive struktur.
Key lighed: Både flydende og faste partikler oplever attraktive kræfter Det holder dem sammen og forhindrer dem i at flygte ind i gasfasen. Styrken af disse kræfter bestemmer stoftilstanden.
 Varme artikler
Varme artikler
-
 UTA tildelte patent for smøremiddelsammensætning til universalfedt til flyPranesh Aswath, førende opfinder for denne forskning og professor i materialevidenskab og teknik og mekanisk og rumfartsteknik. Kredit:University of Texas i Arlington University of Texas i Arlingt
UTA tildelte patent for smøremiddelsammensætning til universalfedt til flyPranesh Aswath, førende opfinder for denne forskning og professor i materialevidenskab og teknik og mekanisk og rumfartsteknik. Kredit:University of Texas i Arlington University of Texas i Arlingt -
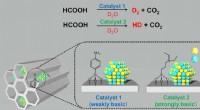 Nanokatalysator gør tungt arbejde af myresyreKontrolleret frigivelse af hydrogenisotopforbindelser fra dehydrogeneringen af myresyre i D 2 O af PdAg-legeringens nanopartikler understøttet på aminfunktionaliseret silica. Kredit:Osaka Universi
Nanokatalysator gør tungt arbejde af myresyreKontrolleret frigivelse af hydrogenisotopforbindelser fra dehydrogeneringen af myresyre i D 2 O af PdAg-legeringens nanopartikler understøttet på aminfunktionaliseret silica. Kredit:Osaka Universi -
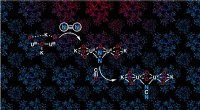 Nitrogenfiksering under omgivende forholdDen oxo-broforbundne uranforbindelse fanger dinitrogen og omdanner dinitrogen og kulilte til cyanamid. Kredit:Marta Falcone/Marinella Mazzanti/EPFL Rigelig i atmosfæren, kvælstof bruges sjældent t
Nitrogenfiksering under omgivende forholdDen oxo-broforbundne uranforbindelse fanger dinitrogen og omdanner dinitrogen og kulilte til cyanamid. Kredit:Marta Falcone/Marinella Mazzanti/EPFL Rigelig i atmosfæren, kvælstof bruges sjældent t -
 Forskere tilbyder virksomheder en ny kemi for grønnere polyurethanEn banebrydende formel for vedvarende energi-NREL-forsker Tao Dong (højre) og tidligere praktikant Stephanie Federle (til venstre) undersøger biobaseret, ikke -toksisk polyurethanharpiks, et lovende a
Forskere tilbyder virksomheder en ny kemi for grønnere polyurethanEn banebrydende formel for vedvarende energi-NREL-forsker Tao Dong (højre) og tidligere praktikant Stephanie Federle (til venstre) undersøger biobaseret, ikke -toksisk polyurethanharpiks, et lovende a
- Stenpermeabilitet, mikroskælvsforbindelse kan være en velsignelse for geotermisk energi
- Hvad er den nøjagtige breddegrad og længdegrad på Fiji -øerne?
- Virkningerne af bioakkumulering på økosystemet
- Hvordan bruger man et mikroskop?
- Hvis mennesker med indlæringsvanskeligheder ikke kan give samtykke til at gifte sig, de er i fare f…
- Ny trussel mod Victoriasøen?


