Hvad sker der med mængden af faste stoffer væsker og gasser, når de varmes køligt?
faste stoffer:
* Opvarmning: De fleste faste stoffer ekspanderer, når de opvarmes. Dette skyldes, at den øgede termiske energi får molekylerne til at vibrere mere kraftigt, hvilket øger den gennemsnitlige afstand mellem dem.
* afkøling: Faststoffer sammentrækkes generelt, når de afkøles. Molekylerne vibrerer mindre, hvilket fører til et fald i den gennemsnitlige afstand.
væsker:
* Opvarmning: Væsker ekspanderer også, når de opvarmes, selvom de typisk er mindre end faste stoffer. Den øgede energi giver molekyler mulighed for at bevæge sig mere frit, hvilket fører til større afstand.
* afkøling: Væsker kontrakt, når de afkøles.
Gasser:
* Opvarmning: Gasser ekspanderer markant, når de opvarmes. Dette skyldes, at gasmolekyler allerede er langt fra hinanden, og den øgede termiske energi får dem til at bevæge sig hurtigere og kollidere oftere og skubber mod containervæggene.
* afkøling: Gasser kontrakt, når de afkøles. Molekylerne bremser ned og kolliderer sjældnere, hvilket fører til et fald i tryk og volumen.
Nøglepunkter:
* termisk ekspansion: Tendensen til stof til at ændre volumen med temperaturændringer kaldes termisk ekspansion.
* Undtagelser: Der er nogle undtagelser fra disse generelle regler. For eksempel udvides vand, når det fryser, hvilket gør det mindre tæt som is.
* applikationer: At forstå termisk ekspansion er afgørende i mange tekniske applikationer, fra at designe broer til bygning af skyskrabere.
Fortæl mig, hvis du gerne vil dykke ned i nogen af disse emner mere detaljeret!
Sidste artikelHvad kaldes materialer med lav modstand?
Næste artikelHvornår kan der skrives resonansstrukturer til et molekyle?
 Varme artikler
Varme artikler
-
 Fremtidens plastik vil leve mange tidligere liv takket være kemisk genbrugDetaljebillede af genbrugsplast. Kredit:Patrick Campbell / University of Colorado Boulder En dag i en ikke alt for fjern fremtid kan plastikken i vores satellitter, biler og elektronik alle leve de
Fremtidens plastik vil leve mange tidligere liv takket være kemisk genbrugDetaljebillede af genbrugsplast. Kredit:Patrick Campbell / University of Colorado Boulder En dag i en ikke alt for fjern fremtid kan plastikken i vores satellitter, biler og elektronik alle leve de -
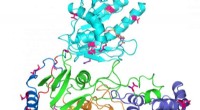 Zika -virusprotein kortlagt til hurtigere søgning efter helbredelseStrukturen af Zika -virusproteinet NS5, hvilket er nøglen til reproduktion og spredning af virussen. Kredit:Cheng Kao, Indiana University En undersøgelse offentliggjort i dag viser, hvordan fors
Zika -virusprotein kortlagt til hurtigere søgning efter helbredelseStrukturen af Zika -virusproteinet NS5, hvilket er nøglen til reproduktion og spredning af virussen. Kredit:Cheng Kao, Indiana University En undersøgelse offentliggjort i dag viser, hvordan fors -
 Forskere skaber holdbare, vaskbar tekstilbelægning, der kan afvise virusEn illustration viser det behandlede tekstils evne til at afvise væsker. Kredit:University of Pittsburgh Masker, kjoler, og andet personligt beskyttelsesudstyr (PPE) er afgørende for at beskytte s
Forskere skaber holdbare, vaskbar tekstilbelægning, der kan afvise virusEn illustration viser det behandlede tekstils evne til at afvise væsker. Kredit:University of Pittsburgh Masker, kjoler, og andet personligt beskyttelsesudstyr (PPE) er afgørende for at beskytte s -
 Nyt krystallinsk oxid kan løse problemet med overophedning i kompositmaterialerKredit:Toshihiro Isobe, Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har for nylig syntetiseret et nyt materiale, der viser unikke termiske ekspansionsegenskaber. Metod
Nyt krystallinsk oxid kan løse problemet med overophedning i kompositmaterialerKredit:Toshihiro Isobe, Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har for nylig syntetiseret et nyt materiale, der viser unikke termiske ekspansionsegenskaber. Metod
- Matematik afslører ny indsigt i Marangoni-strømme
- Rigid beslutningstagning kan skade samvittighedsfulde medarbejdere
- Dyb læring vil hjælpe fremtidige Mars-rovere med at gå længere, hurtigere, og lave mere videnska…
- Første gamle dyrkede ris opdaget i Centralasien
- Robotsyn gør solcelleproduktion mere effektiv
- En harmløs asteroide vil suse forbi Jorden lørdag. Sådan får du øje på det


