Hvorfor er forbindelser gode isolatorer?
Her er en sammenbrud:
Hvorfor nogle forbindelser er gode isolatorer:
* stærke kovalente obligationer: Forbindelser med stærke kovalente bindinger, som diamant eller mange polymerer, har elektroner tæt bundet til atomerne. Disse elektroner er ikke fri til at bevæge sig og forhindrer strømmen af elektricitet.
* Stort båndgap: Den energi, der kræves for at flytte et elektron fra valensbåndet til ledningsbåndet (hvor det kan udføre elektricitet) er høj i mange forbindelser. Dette "båndgap" gør det vanskeligt for elektroner at få nok energi til at blive fri og opførsel.
* Mangel på gratis ladningsbærere: Mange forbindelser har ikke frie elektroner eller ioner, der let kan bevæge og bære elektrisk strøm.
Hvorfor nogle forbindelser er gode ledere:
* ioniske forbindelser: Forbindelser med ioniske bindinger har ladet ioner, der kan bevæge sig frit, når de opløses i vand eller smeltes. Denne bevægelse giver mulighed for strøm af elektricitet.
* Metalliske forbindelser: Metaller har et "hav af elektroner", hvor elektroner er løst bundet og kan bevæge sig frit, hvilket gør dem til fremragende ledere.
Eksempler:
* gode isolatorer: Diamant, gummi, glas, plastik
* Gode ledere: Salt (NaCl), kobber, guld
Afslutningsvis bestemmes den elektriske ledningsevne af en forbindelse af dens kemiske struktur, bindingstype og tilstedeværelsen af frie ladningsbærere.
Det er vigtigt at bemærke, at nogle forbindelser kan fungere som halvledere , hvilket betyder, at de kan udføre elektricitet under visse betingelser, men ikke andre. Dette skyldes faktorer som temperatur, doping og urenheder.
Sidste artikelProducerer atomkraft sur regn?
Næste artikelHvad er nogle egenskaber ved molekylære forbindelser?
 Varme artikler
Varme artikler
-
 Forskere løser kontroverser om energigabet i Van der Waals-materialeTeYu Chien, en University of Wyoming lektor i fysik og astronomi, og Dinesh Baral, en UW kandidatstuderende, ledet forskning, der brugte scanning tunneling mikroskopi og spektroskopi målinger, der kla
Forskere løser kontroverser om energigabet i Van der Waals-materialeTeYu Chien, en University of Wyoming lektor i fysik og astronomi, og Dinesh Baral, en UW kandidatstuderende, ledet forskning, der brugte scanning tunneling mikroskopi og spektroskopi målinger, der kla -
 Video:Heltinder i det periodiske systemKredit:The American Chemical Society I 1871, Dimitri Mendeleev præsenterede sit periodiske system for verden. Mange af de nuværende 118 elementer manglede, og han efterlod pladsholdere til dem, de
Video:Heltinder i det periodiske systemKredit:The American Chemical Society I 1871, Dimitri Mendeleev præsenterede sit periodiske system for verden. Mange af de nuværende 118 elementer manglede, og han efterlod pladsholdere til dem, de -
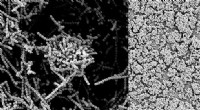 Sukker i modermælk er en ny klasse af antibakterielle midlerNærbilledet til venstre illustrerer, hvordan Strep-bakterier normalt klumper sig sammen for at danne en beskyttende biofilm. Billedet til højre viser, at biofilmen nedbrydes, når en Strep-kultur doser
Sukker i modermælk er en ny klasse af antibakterielle midlerNærbilledet til venstre illustrerer, hvordan Strep-bakterier normalt klumper sig sammen for at danne en beskyttende biofilm. Billedet til højre viser, at biofilmen nedbrydes, når en Strep-kultur doser -
 Græs erstatter plast i take-away mademballageKredit:CC0 Public Domain Græsfibre kan erstatte plastik som et 100 % biologisk nedbrydeligt og engangsmateriale til emballering til take-away mad. Dette er målet for det nye innovative projekt Sin
Græs erstatter plast i take-away mademballageKredit:CC0 Public Domain Græsfibre kan erstatte plastik som et 100 % biologisk nedbrydeligt og engangsmateriale til emballering til take-away mad. Dette er målet for det nye innovative projekt Sin
- En lavine demonstrerer, hvilken slags energi der skal varmeenergi?
- Lys udløser guld på uventet vis
- Amerikansk astronaut, der opsender næste måned, kan tilbringe et år i rummet
- Hvad er et virkeligt eksempel på cinderkegle vulkan?
- Tidssymmetri og fysikkens love
- Udviser en levende organisme alle egenskaberne liv?


