Hvilke to måder opfører elektroner?
1. bølgepartikel dualitet: Dette er hjørnestenen i kvantemekanik. Elektroner kan fungere som både bølger og partikler, afhængigt af situationen.
* bølgelignende opførsel: Elektroner kan diffrere og blande sig som lette bølger. Dette observeres i fænomener som det dobbelt-spalte eksperiment.
* Partikellignende opførsel: Elektroner kan lokaliseres og interagerer med andre partikler som diskrete enheder. Dette er tydeligt i deres opførsel i kredsløb og atomstruktur.
2. Kvantisering: Elektroner kan kun eksistere i specifikke energiniveauer inden for et atom eller molekyle. Dette betyder, at deres energi er kvantiseret, hvilket betyder, at den kun kan påtage sig diskrete værdier.
* Energiniveau: Elektroner hopper mellem disse energiniveau ved at absorbere eller udsende fotoner af specifikke energier. Dette er grundlaget for atomspektroskopi.
Disse to opførsler er vigtige for at forstå elektronernes opførsel i forskellige sammenhænge, fra den mikroskopiske verden af atomer til den makroskopiske verden af elektronik.
Sidste artikelHvilken type varme overføres gennem gasser?
Næste artikelEr tåge en fast væske eller gas?
 Varme artikler
Varme artikler
-
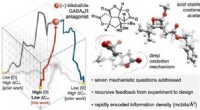 Kemikere udvikler rammer for at muliggøre effektiv syntese af informationstætte molekylerKredit:ACS Et team ledet af forskere ved Scripps Research har udviklet en teoretisk tilgang, der kan lette processen med at gøre meget kompleks, kompakte molekyler. Sådanne molekyler findes ofte
Kemikere udvikler rammer for at muliggøre effektiv syntese af informationstætte molekylerKredit:ACS Et team ledet af forskere ved Scripps Research har udviklet en teoretisk tilgang, der kan lette processen med at gøre meget kompleks, kompakte molekyler. Sådanne molekyler findes ofte -
 Kunstig fotosyntese kan omdanne ubrugelig kuldioxid til myresyre, der bruges i industrienNaturlig fotosyntese er ikke altid særlig effektiv. Når videnskabsmænd efterligner det, de forsøger at gøre processerne meget mere effektive. Kredit:Colourbox Med energi fra solen, et særligt enzy
Kunstig fotosyntese kan omdanne ubrugelig kuldioxid til myresyre, der bruges i industrienNaturlig fotosyntese er ikke altid særlig effektiv. Når videnskabsmænd efterligner det, de forsøger at gøre processerne meget mere effektive. Kredit:Colourbox Med energi fra solen, et særligt enzy -
 Elbilbatterier inspirerer til sikrere, billigere måde at fremstille forbindelser, der bruges i medi…Forskere ved Scripps Research, inspireret af disse batteriers raffinerede elektrokemi, har udviklet et batterilignende system, der giver dem mulighed for at gøre potentielle fremskridt inden for frems
Elbilbatterier inspirerer til sikrere, billigere måde at fremstille forbindelser, der bruges i medi…Forskere ved Scripps Research, inspireret af disse batteriers raffinerede elektrokemi, har udviklet et batterilignende system, der giver dem mulighed for at gøre potentielle fremskridt inden for frems -
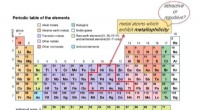 Stærk M-M Pauli frastødning fører til frastødende metallofilicitetPeriodisk system, der viser elementer, der kunne udvise metallofilicitet. Kredit:University of Hong Kong Et forskerhold ledet af professor Chi-Ming Che og Dr. Jun Yang, fra forskningsafdelingen fo
Stærk M-M Pauli frastødning fører til frastødende metallofilicitetPeriodisk system, der viser elementer, der kunne udvise metallofilicitet. Kredit:University of Hong Kong Et forskerhold ledet af professor Chi-Ming Che og Dr. Jun Yang, fra forskningsafdelingen fo
- er målesystemet universelt blandt videnskabsmænd?
- Er underjordisk transit værre for dit helbred?
- 10 funktioner, vi gerne vil se på den næste iPhone
- Facebook tilbyder interaktive spilshows på videoplatformen
- Monsunstorme færre, men mere ekstreme
- Hvorfor pandemien introducerer sprog, der er svært at forklare


