Udvides gas, når den afkøles?
Her er hvorfor:
* gaslov: Gassens opførsel styres af gaslove, primært den ideelle gaslov. Denne lov siger, at mængden af en gas er omvendt proportional til dens temperatur (ved konstant tryk).
* afkøling og volumen: Når du afkøler en gas, reducerer du dens kinetiske energi (bevægelsesenergien for dens molekyler). Dette betyder, at molekylerne bevæger sig langsommere og kolliderer sjældnere med containerens vægge. Som et resultat falder det tryk, der udøves af gassen, og gas kontrakter (dens volumen falder).
Tænk på det på denne måde: Forestil dig en ballon fyldt med luft. Når du lægger ballonen i køleskabet, afkøles luften inde. Molekylerne bremser ned og udøver mindre pres på ballonens indre vægge, hvilket får ballonen til at krympe.
Undtagelser:
* Faseændringer: Mens gas generelt kontrakter, når de afkøles, er der en undtagelse, når gassen når sit kondensationspunkt. På dette tidspunkt kan gasovergange til en flydende tilstand, og dens volumen kan ændres dramatisk.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
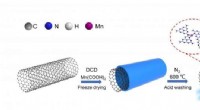 Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne
Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne -
 Processen til at tilpasse molekyler virker dobbeltRice University kandidatstuderende Kang-Jie (Harry) Bian opstiller lysfølsomme molekyler til et eksperiment i laboratoriet hos kemiker Julian West. Bian er hovedforfatter af en undersøgelse inspireret
Processen til at tilpasse molekyler virker dobbeltRice University kandidatstuderende Kang-Jie (Harry) Bian opstiller lysfølsomme molekyler til et eksperiment i laboratoriet hos kemiker Julian West. Bian er hovedforfatter af en undersøgelse inspireret -
 Dødelig fejl afsløret i grøn pigmenteret betonKredit:CC0 Public Domain Da Xian Jiaotong-Liverpool University forskere afsluttede deres forskning om farvet arkitektonisk beton, de fandt et overraskende resultat - grøn pigmenteret cement havde
Dødelig fejl afsløret i grøn pigmenteret betonKredit:CC0 Public Domain Da Xian Jiaotong-Liverpool University forskere afsluttede deres forskning om farvet arkitektonisk beton, de fandt et overraskende resultat - grøn pigmenteret cement havde -
 Genredigeringsteknik gør det muligt for silkeorme at producere edderkoppesilkeEn analyse af transformerede kokoner. Morfologi af WT-1, FibH+/-, FibH-/-, WT-2, MaSp1+/-, og MaSp1+/+ kokoner. Målestok repræsenterer 1 cm. Kredit:Jun Xu Et team af forskere tilknyttet flere inst
Genredigeringsteknik gør det muligt for silkeorme at producere edderkoppesilkeEn analyse af transformerede kokoner. Morfologi af WT-1, FibH+/-, FibH-/-, WT-2, MaSp1+/-, og MaSp1+/+ kokoner. Målestok repræsenterer 1 cm. Kredit:Jun Xu Et team af forskere tilknyttet flere inst
- Forskere udvikler en ny metode til at forringe billeder
- Forekommer nuklearafdelingen i mitose eller intrphase?
- Uret tikker, mens SpaceX bygger fartøjer til NASA
- Går potentiel energi op eller ned?
- Hvorfor er ørne afhængige af sollys for deres energi?
- Sådan tuner du almindelige lugte og fokuserer på vigtige


