Hvorfor er dannelse af anion eksoterm?
Eksotermisk aniondannelse:
* Elektronaffinitet: Dette henviser til energien frigivet Når et atom får et elektron til at danne en negativ ion. En højere elektronaffinitet indikerer en mere eksoterm proces.
* Elektrostatisk attraktion: Når et atom får et elektron, tiltrækkes den negativt ladede elektron af den positivt ladede kerne og frigiver energi.
* stabilitet: Atomer bliver ofte mere stabile ved at opnå en fuld ydre elektronskal. Denne stabilitet ledsages ofte af frigivelse af energi.
endotermisk aniondannelse:
* frastødning: Når et atom får flere elektroner, afviser de tilsatte elektroner hinanden. Denne frastødelse kræver energiindgang, hvilket gør processen endotermisk. Dette gælder især for elementer med allerede store negative afgifter.
* Elektronkonfiguration: Nogle gange destabiliseres tilsætning af et elektron til et atom * * dens elektronkonfiguration. Dette er tilfældet for elementer som de ædle gasser, som allerede er meget stabile.
Nøglefaktorer, der påvirker aniondannelsen:
* atomstørrelse: Mindre atomer har generelt en højere elektronaffinitet, fordi den indkommende elektron er tættere på kernen og oplever en stærkere attraktion.
* atomafgift: En højere atomafgift tiltrækker elektroner stærkere, hvilket fører til en mere eksoterm proces.
* Elektronkonfiguration: Atomer med elektronkonfigurationer tæt på en fyldt skal er mere tilbøjelige til at få elektroner eksotermisk.
Som konklusion, mens mange anionformationer er eksoterme på grund af faktorer som elektronaffinitet og elektrostatisk attraktion, er der undtagelser. Den endotermiske karakter af nogle aniondannelsesprocesser skyldes faktorer som elektronafvisning og destabiliserende elektronkonfigurationer.
Sidste artikelBeskriv bindingen i et vandmolekyle?
Næste artikelHvad er rolle i organiske molekyler?
 Varme artikler
Varme artikler
-
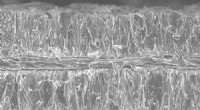 Galvanisering giver høj energi, højeffekts batterierEt elektronmikrografi-tværsnit viser aluminiumsfolie belagt med lithium-koboltoxid, et almindeligt materiale i lithium-ion-batterier. Kredit:Billede udlånt af Hailong Ning og Jerome Davis III, Xerion
Galvanisering giver høj energi, højeffekts batterierEt elektronmikrografi-tværsnit viser aluminiumsfolie belagt med lithium-koboltoxid, et almindeligt materiale i lithium-ion-batterier. Kredit:Billede udlånt af Hailong Ning og Jerome Davis III, Xerion -
 ORNL opfylder FDA's vigtigste milepæl for kræftbekæmpende Ac-225 isotopMålrettet alfaterapi kan levere stråling til specifikke celler, med minimal indvirkning på omgivelserne, sunde celler. Kredit:Michelle Lehman og Jaimee Janiga/ORNL, US Department of Energy En sjæl
ORNL opfylder FDA's vigtigste milepæl for kræftbekæmpende Ac-225 isotopMålrettet alfaterapi kan levere stråling til specifikke celler, med minimal indvirkning på omgivelserne, sunde celler. Kredit:Michelle Lehman og Jaimee Janiga/ORNL, US Department of Energy En sjæl -
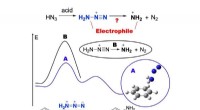 Kemikere beviser mekanismen for direkte aminering fra benzenDet grafiske abstrakt af direkte aminering. Kredit:Tomsk Polytechnic University (TPU) Et team af kemikere fra Tomsk Polytekniske Universitet opdagede en mekanisme for direkte elektrofil aminering
Kemikere beviser mekanismen for direkte aminering fra benzenDet grafiske abstrakt af direkte aminering. Kredit:Tomsk Polytechnic University (TPU) Et team af kemikere fra Tomsk Polytekniske Universitet opdagede en mekanisme for direkte elektrofil aminering -
 Præcisionseksperimenter afslører huller i van der Waals teoriKredit:University of Tsukuba Opdagelsen af grafen, med sit høje styrke-til-vægt-forhold, fleksibilitet, elektrisk ledningsevne, og evnen til at danne en uigennemtrængelig barriere, førte til en
Præcisionseksperimenter afslører huller i van der Waals teoriKredit:University of Tsukuba Opdagelsen af grafen, med sit høje styrke-til-vægt-forhold, fleksibilitet, elektrisk ledningsevne, og evnen til at danne en uigennemtrængelig barriere, førte til en
- Hvorfor afkøles mælken, før der tilsættes bakterier?
- Tværfaglig tilgang er den eneste måde at imødegå ødelæggende virkninger af jorderosion
- Undersøgelsen identificerer et stigende behov for at ansætte dataanalytikere til offentlige job
- Knirkende gulve fungerede som sikkerhedsadvarselssystem i det gamle Japan
- Elliott investerer 3,2 mia. USD i AT&T, søger ændringer
- At ændre, hvad vi spiser, kan opveje årevis med klimaopvarmende emissioner, nye analysefund


