Forståelse af vands opløsningsmiddelegenskaber:Opløsning af ioner
* Polaritet: Vandmolekyler er bøjet, hvor oxygenatomet har en delvis negativ ladning og hydrogenatomerne har delvist positive ladninger. Dette skaber et dipolmoment, hvilket gør vand til et polært molekyle.
* Brintbinding: De delvise positive ladninger på vandmolekylernes brintatomer kan danne stærke brintbindinger med de negative ioner. På samme måde kan den delvise negative ladning på oxygenatomet interagere med positive ioner.
* Løsning: Når en ionforbindelse opløses i vand, omgiver de polære vandmolekyler de individuelle ioner og adskiller dem effektivt fra hinanden. De positive ender af vandmolekyler omgiver de negative ioner og omvendt. Denne proces kaldes løsning .
Her er grunden til, at disse egenskaber gør vand til et godt opløsningsmiddel for ioner:
* Attraktive kræfter: Den stærke elektrostatiske tiltrækning mellem de polære vandmolekyler og ionerne overvinder de kræfter, der holder den ioniske forbindelse sammen.
* Spredning: Solvateringsprocessen spreder effektivt ionerne i vandet og forhindrer dem i at rekombinere og danne et fast stof igen.
Opsummering: Vands polaritet og evne til at danne hydrogenbindinger gør det muligt for det at omgive og isolere ioner, hvilket gør det til et fremragende opløsningsmiddel for ioniske forbindelser.
 Varme artikler
Varme artikler
-
 Forskere opdager en bedre måde at lave plast af svovl påKredit:CC0 Public Domain Forskere ved University of Liverpool har opdaget en ny proces til fremstilling af polymerer af svovl, som kan være en måde at fremstille plast på, der er mindre skadeligt
Forskere opdager en bedre måde at lave plast af svovl påKredit:CC0 Public Domain Forskere ved University of Liverpool har opdaget en ny proces til fremstilling af polymerer af svovl, som kan være en måde at fremstille plast på, der er mindre skadeligt -
 Hvad er bevaret i kemiske reaktioner? Forståelse af loven om bevaring af stofferAf David Dunning, opdateret 30. august 2022 Bevarelse af stof Kemiens grundlæggende princip, Loven om Materiens Bevarelse, siger, at stof ikke kan skabes eller ødelægges i et lukket system. I en typi
Hvad er bevaret i kemiske reaktioner? Forståelse af loven om bevaring af stofferAf David Dunning, opdateret 30. august 2022 Bevarelse af stof Kemiens grundlæggende princip, Loven om Materiens Bevarelse, siger, at stof ikke kan skabes eller ødelægges i et lukket system. I en typi -
 Lego-lignende kemiske byggeklodser samler sig selv til katalysator til brintbrændselscellerDen nye katalysator, en cofacial kobolt porphyrin, er skabt ved hjælp af en proces kaldet molekylær selvsamling. Under denne proces, et hætteglas fyldt med molekyler kaldet koboltporphyriner (hættegla
Lego-lignende kemiske byggeklodser samler sig selv til katalysator til brintbrændselscellerDen nye katalysator, en cofacial kobolt porphyrin, er skabt ved hjælp af en proces kaldet molekylær selvsamling. Under denne proces, et hætteglas fyldt med molekyler kaldet koboltporphyriner (hættegla -
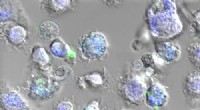 En ny slags vaccine baseret på edderkoppesilkeImmunceller, der indtog nanopartikler af edderkoppesilke (i grønt). Endosomerne - den del af cellen, hvori nanopartiklerne frigiver vaccinen - vises i blåt. Kredit:Laboratoire Bourquin – UNIGE For
En ny slags vaccine baseret på edderkoppesilkeImmunceller, der indtog nanopartikler af edderkoppesilke (i grønt). Endosomerne - den del af cellen, hvori nanopartiklerne frigiver vaccinen - vises i blåt. Kredit:Laboratoire Bourquin – UNIGE For
- Hvad er pointgruppen for benzen?
- Love Island:De psykologiske udfordringer, deltagere og seere kan stå over for, efter showet er slut
- Langsigtet satellitanalyse viser regntiden vådere nu end nogensinde
- Forskere finder en måde at forbinde kvante og klassisk fysik
- Startede kometer livet på Jorden? Kemikere finder en manglende puslespil
- Isotopanalyse peger på Maya-krigsfanger


