Ammonium og hydroxid:syre vs. baseegenskaber forklaret
* Ammonium (NH4+) er ikke en syre i sig selv. Det er en kation , hvilket betyder, at den har en positiv ladning. Det kan dog fungere som en svag syre i opløsning. Dette skyldes, at det kan donere en proton (H⁺) til vandmolekyler:
NH4⁺ + H₂O⇌ NH₃ + H3O⁺
* Hydroxid (OH⁻) er ikke en base i sig selv er det en anion , hvilket betyder, at den har en negativ ladning. Det er dog en stærk base i opløsning. Det accepterer direkte protoner (H⁺) fra vandmolekyler:
OH⁻ + H2O ⇌ H2O + OH⁻
Nøglepunkter:
* Syrer donere protoner (H⁺).
* Baser acceptere protoner (H⁺).
* Kationer er positivt ladede ioner.
* Anioner er negativt ladede ioner.
Så mens ammonium og hydroxid ikke er syrer og baser i sig selv, kan de fungere som sådan i opløsning.
Sidste artikelAmmoniumhydroxid vs. natriumhydroxid:Forståelse af basestyrke
Næste artikelForståelse af ammoniumhydroxid:ioner og egenskaber
 Varme artikler
Varme artikler
-
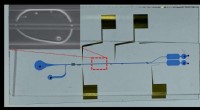 Mikrofluidisk system med celleadskillende kræfter kan afsløre, hvordan nye patogener angriberEt billede af den in-dråbe celleadskillelse mikrofluidisk chip, viser de mikrofluidiske kanaler og elektroder. Forstørret billede viser en værtscelle og patogene bakterieceller, der adskilles til top
Mikrofluidisk system med celleadskillende kræfter kan afsløre, hvordan nye patogener angriberEt billede af den in-dråbe celleadskillelse mikrofluidisk chip, viser de mikrofluidiske kanaler og elektroder. Forstørret billede viser en værtscelle og patogene bakterieceller, der adskilles til top -
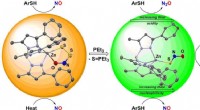 Sporing af nitrogenoxid-signalvejenKredit:Wiley Både nitrogenoxid (NO) og svovlbrinte (H 2 S) fungerer som gasformige signalmolekyler med lignende fysiologiske virkninger. Mange af de kritiske spørgsmål om samspillet mellem disse
Sporing af nitrogenoxid-signalvejenKredit:Wiley Både nitrogenoxid (NO) og svovlbrinte (H 2 S) fungerer som gasformige signalmolekyler med lignende fysiologiske virkninger. Mange af de kritiske spørgsmål om samspillet mellem disse -
 Nyt kvantemateriale kan advare om neurologisk sygdomDet sorte rektangel under disse guldtrin er et nyt kvantemateriale, der er i stand til at lytte til hjernen ved at gribe atomer, som hjernen naturligt bruger til at kommunikere. Kredit:Purdue Universi
Nyt kvantemateriale kan advare om neurologisk sygdomDet sorte rektangel under disse guldtrin er et nyt kvantemateriale, der er i stand til at lytte til hjernen ved at gribe atomer, som hjernen naturligt bruger til at kommunikere. Kredit:Purdue Universi -
 Et bedre bæredygtigt hygiejnebindSHERO Pad, udviklet af et team af University of Utah materialevidenskab og ingeniørstuderende, er en ny feminin hygiejnepude, der er 100 procent biologisk nedbrydelig og lavet af alle naturlige materi
Et bedre bæredygtigt hygiejnebindSHERO Pad, udviklet af et team af University of Utah materialevidenskab og ingeniørstuderende, er en ny feminin hygiejnepude, der er 100 procent biologisk nedbrydelig og lavet af alle naturlige materi
- Hvad opdagede Hubble som et resultat af at studere de røde skift fjerne galakser?
- NASA gør status over planteplanktonpopulationer i Stillehavet
- Hvilken slags organismer udviser gametisk meiose?
- PhenoCam -netværk udnytter store data til at forudsige indvirkningen af varmere klima på økosys…
- Rumfirmaer ser lanceringsrisiko fra lav iltforsyning midt i pandemi
- Udbryderpartier truer med at forstyrre Sydkoreas topartisystem. Kan de også bringe den parlamentari…


