Flammetestfarver:Forståelse af atomemission
1. Varme og excitation: Når et metalsalt opvarmes i en flamme, giver den høje temperatur energi nok til at excitere elektronerne i metalionerne. Disse elektroner hopper til højere energiniveauer.
2. Tilbage til grundtilstand: Exciterede elektroner er ustabile og ønsker at vende tilbage til deres oprindelige, lavere energiniveauer (grundtilstand). For at gøre dette frigiver de den overskydende energi som lys.
3. Unikke bølgelængder: Energiforskellen mellem den exciterede tilstand og grundtilstanden er specifik for hvert element. Denne energiforskel svarer til en bestemt bølgelængde af lys. Da forskellige grundstoffer har unikke energiniveauer, udsender de lys i forskellige farver.
Opsummering:
* Varme: Giver energi til elektroner til at hoppe til højere niveauer.
* Elektronovergange: Elektroner hopper ned igen og frigiver energi som lys.
* Bølgelængde: Den frigivne energi svarer til en bestemt bølgelængde af lys, der bestemmer den farve, vi ser.
Eksempel:
* Natrium: Natriumioner udsender gult lys, fordi energiforskellen mellem deres exciterede tilstand og grundtilstand svarer til bølgelængden af gult lys.
* Kobber: Kobberioner udsender blågrønt lys, fordi energiforskellen for kobber er i den blågrønne del af det synlige spektrum.
Vigtig bemærkning: Farven observeret i en flammetest kan være påvirket af faktorer som tilstedeværelsen af andre elementer i prøven og flammens temperatur. Princippet om elektroniske overgange forbliver dog det samme, hvilket giver et unikt "fingeraftryk" for hvert element.
Sidste artikelForstå farven på stærke alkalier:En omfattende guide
Næste artikelKF (kaliumfluorid):Ionbindingsdannelse forklaret
 Varme artikler
Varme artikler
-
 Forskere opdager, at traditionelle væskestrømobservationer kan gå glip af det store billedeEn tidsmæssig reaktion opstod under væskestrømmen indikerede en grundlæggende strukturændring i væskerne. Kredit:Figur tilpasset med tilladelse fra forsiden af J. Phys. Chem. B 2019, 123, 21, 4587-4
Forskere opdager, at traditionelle væskestrømobservationer kan gå glip af det store billedeEn tidsmæssig reaktion opstod under væskestrømmen indikerede en grundlæggende strukturændring i væskerne. Kredit:Figur tilpasset med tilladelse fra forsiden af J. Phys. Chem. B 2019, 123, 21, 4587-4 -
 En speciel elementær magiProtoner har forskellige stabile magiske tal:2, 8, 20, 28, og så videre. Når nukleare baner er fyldt med protoner, de danner stabile kerner, analogt med ædelgaselementerne Kredit:Kyoto University/Yosh
En speciel elementær magiProtoner har forskellige stabile magiske tal:2, 8, 20, 28, og så videre. Når nukleare baner er fyldt med protoner, de danner stabile kerner, analogt med ædelgaselementerne Kredit:Kyoto University/Yosh -
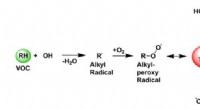 Identifikation af et undvigende molekyle nøgle til forbrændingskemiEt diagram, der viser, hvordan oxidationen af flygtige organiske forbindelser (VOC) kan forbruge og regenerere OH-radikaler. Et alkylradikal (R•) reagerer med oxygen og danner et alkylperoxyradikal
Identifikation af et undvigende molekyle nøgle til forbrændingskemiEt diagram, der viser, hvordan oxidationen af flygtige organiske forbindelser (VOC) kan forbruge og regenerere OH-radikaler. Et alkylradikal (R•) reagerer med oxygen og danner et alkylperoxyradikal -
 Ny biobrændstofteknologi reducerer produktionstiden markantCigdem Eskicioglu er professor i ingeniørvidenskab ved UBCs Okanagan Campus. Kredit:UBC Okanagan Ny forskning fra en professor i teknik på UBCs Okanagan Campus kan indeholde nøglen til biobrændsto
Ny biobrændstofteknologi reducerer produktionstiden markantCigdem Eskicioglu er professor i ingeniørvidenskab ved UBCs Okanagan Campus. Kredit:UBC Okanagan Ny forskning fra en professor i teknik på UBCs Okanagan Campus kan indeholde nøglen til biobrændsto
- Den største flyvende fugl nogensinde:En 21 fods bevinget forhistorisk kæmpe, der overskygger moder…
- Hvad betyder reduktion af genbrug og recylcle?
- Hvordan løser man en ubalanceret kemisk ligning?
- Hvordan er planteceller dyr og bakterie?
- Indstilling af en TRAP for pandemi-fremkaldende vira
- Hvad er den højeste højde over middagssol fra 35. breddegrad?


