Ammoniak- og svovlsyrereaktion:Kemi, ligning og forklaring
Her er den afbalancerede kemiske ligning:
2 NH3 + H2SO4 → (NH4)2SO4
Forklaring:
* Ammoniak (NH₃) er en svag base, hvilket betyder, at den accepterer protoner (H⁺).
* Svovlsyre (H2SO4) er en stærk syre, hvilket betyder, at den let donerer protoner (H⁺).
Når ammoniak og svovlsyre reagerer, accepterer ammoniakmolekylerne protoner fra svovlsyren og danner ammoniumioner (NH4⁺). Denne proces efterlader sulfationer (SO₄²⁻), som kombineres med ammoniumionerne og danner ammoniumsulfat ((NH4)₂SO4).
Nøglepunkter:
* Reaktionen er meget eksoterm og frigiver varme.
* Ammoniumsulfat er et salt, der almindeligvis bruges som gødning.
* Reaktionen er reversibel, men ligevægten ligger langt til højre og begunstiger dannelsen af ammoniumsulfat.
Denne reaktion er et klassisk eksempel på syre-base kemi, der demonstrerer neutraliseringen af en syre med en base.
 Varme artikler
Varme artikler
-
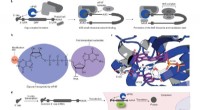 Biokemikere bruger nyt værktøj til at kontrollere mRNA ved hjælp af lys5′-hætten er et kendetegn for eukaryote mRNAer, der styrer translationsinitiering. a, Nøgletrin i oversættelsesinitiering. Den eukaryote translationsinitieringsfaktor eIF4E binder direkte til 5′-hætte
Biokemikere bruger nyt værktøj til at kontrollere mRNA ved hjælp af lys5′-hætten er et kendetegn for eukaryote mRNAer, der styrer translationsinitiering. a, Nøgletrin i oversættelsesinitiering. Den eukaryote translationsinitieringsfaktor eIF4E binder direkte til 5′-hætte -
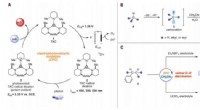 Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi
Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi -
 Urankemi og geologisk deponering af radioaktivt affaldDemonstration af en prøve, der indeholder uran, studeres og omhyggeligt indlæses på Diamonds I20-scanningsstrålelinje - Credit Diamond Light Source Kredit:Diamond Light Source Et nyt papir, der ud
Urankemi og geologisk deponering af radioaktivt affaldDemonstration af en prøve, der indeholder uran, studeres og omhyggeligt indlæses på Diamonds I20-scanningsstrålelinje - Credit Diamond Light Source Kredit:Diamond Light Source Et nyt papir, der ud -
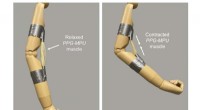 Højenergi formhukommelsespolymer kunne en dag hjælpe robotter med at bøje deres musklerEn kunstig muskel lavet af en strakt formhukommelsespolymer trækker sig sammen ved opvarmning, bøjer en mannequin arm. Kredit:Tilpasset fra ACS Central Science 2021, DOI:10.1021/acscentsci.1c00829
Højenergi formhukommelsespolymer kunne en dag hjælpe robotter med at bøje deres musklerEn kunstig muskel lavet af en strakt formhukommelsespolymer trækker sig sammen ved opvarmning, bøjer en mannequin arm. Kredit:Tilpasset fra ACS Central Science 2021, DOI:10.1021/acscentsci.1c00829
- Hvad er alkoholholdig og mælkesyre fermentering?
- Hvilke ting har strålende energi?
- Hvad er langsom massebevægelse?
- Kigger uden for fiberen:Forskere demonstrerer nyt koncept for optiske fibersensorer
- Catalina-hjort i trådkorset:Vil kompromis afværge en planlagt slagtning?
- En ny model for gruppebeslutningstagning viser, hvordan følgere kan påvirke resultatet


