Klorgasdensitetsberegner:Beregn massefylde ved 7,50 x 10^2 Torr &25°C
1. Konverter tryk til atmosfærer:
* 1 atm =760 torr
* 7,50 x 10² torr * (1 atm / 760 torr) =0,987 atm
2. Konverter temperatur til Kelvin:
*K =°C + 273,15
* 25,0 °C + 273,15 =298,15 K
3. Brug den ideelle gaslov:
Den ideelle gaslov relaterer tryk (P), volumen (V), antal mol (n), den ideelle gaskonstant (R) og temperatur (T):
* PV =nRT
For at finde massefylde (ρ), skal vi omarrangere ligningen for at løse for masse (m) over volumen (V):
* ρ =m/V
Vi kan relatere masse til mol ved at bruge den molære masse (M) af klorgas (Cl₂):
*m =nM
Erstat nu disse forhold med den ideelle gaslov:
* P(V) =(m/M)RT
* PV =(ρV)RT/M
* ρ =(PM) / (RT)
4. Tilslut værdierne og beregn:
* P =0,987 atm
* M =70,90 g/mol (molær masse af Cl2)
* R =0,0821 L·atm/mol·K
* T =298,15 K
ρ =(0,987 atm * 70,90 g/mol) / (0,0821 L·atm/mol·K * 298,15 K)
ρ ≈ 2,85 g/L
Derfor er tætheden af klorgas ved 7,50 x 10² torr og 25,0 °C ca. 2,85 g/L.
 Varme artikler
Varme artikler
-
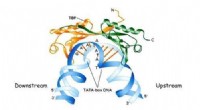 Syntetisk præget polymerer genkendt af DNAKredit:University of North Texas En UNT -kemiker er en del af et internationalt team, der netop har fået et gennembrud inden for DNA -forskning. Ved hjælp af en polymermatrix, holdet var i stand t
Syntetisk præget polymerer genkendt af DNAKredit:University of North Texas En UNT -kemiker er en del af et internationalt team, der netop har fået et gennembrud inden for DNA -forskning. Ved hjælp af en polymermatrix, holdet var i stand t -
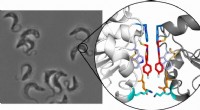 Ny terapeutisk tilgang til bekæmpelse af afrikansk sovesygeTrypanosomer, som forårsager afrikansk sovesyge, under mikroskopet (til venstre) og krystalstrukturen af tryparedoxin-dimeren (til højre):De to inhibitormolekyler er fremhævet med rødt. Kredit:Ute H
Ny terapeutisk tilgang til bekæmpelse af afrikansk sovesygeTrypanosomer, som forårsager afrikansk sovesyge, under mikroskopet (til venstre) og krystalstrukturen af tryparedoxin-dimeren (til højre):De to inhibitormolekyler er fremhævet med rødt. Kredit:Ute H -
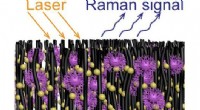 En hurtig og billig enhed til at fange og identificere viraArray af nanorør dekoreret med guld nanopartikler fanger virusmolekyler. Kredit:Terrones Lab/Penn State En enhed til hurtigt at fange og identificere forskellige virusstammer er blevet udviklet, i
En hurtig og billig enhed til at fange og identificere viraArray af nanorør dekoreret med guld nanopartikler fanger virusmolekyler. Kredit:Terrones Lab/Penn State En enhed til hurtigt at fange og identificere forskellige virusstammer er blevet udviklet, i -
 Hurtig, præcis og ikke-destruktiv:Den nye metode til at analysere fødevarekvalitetNIRS analyse af spinatplanter direkte i marken. Kredit:Universidad de Córdoba Forbrugerne leder altid efter produkter af god kvalitet, frem for alt i frisk mad som grøntsager. Men hvordan måler vi
Hurtig, præcis og ikke-destruktiv:Den nye metode til at analysere fødevarekvalitetNIRS analyse af spinatplanter direkte i marken. Kredit:Universidad de Córdoba Forbrugerne leder altid efter produkter af god kvalitet, frem for alt i frisk mad som grøntsager. Men hvordan måler vi
- Lysets håndhævelse er nøglen til bedre optisk kontrol
- Hvordan man bevarer virksomhedens værdi under fusioner og opkøb
- Undersøgelser giver en bedre forståelse af, hvordan cyanobakterier udnytter glukose
- Forskere opdager, hvordan en gruppe larver blev giftige
- Indeholder energi frigivet fra ATP fem fosfatgrupper?
- Hvilken type transport finder sted, når et protein tillader en ion at komme ind i celle, men der er…


