Bestemmelse af den empiriske formel for et kulstofrigt kulbrinte
1. Antag en prøve på 100 g
* Dette gør beregningerne nemmere, da procenterne direkte oversættes til gram.
* Du har 85,7 g kulstof og (100 - 85,7) =14,3 g brint.
2. Konverter gram til mol
* Brug den molære masse af hvert element:
* Kulstof (C):12,01 g/mol
* Brint (H):1,01 g/mol
* Mol kulstof:85,7 g / 12,01 g/mol =7,14 mol
* Mol brint:14,3 g / 1,01 g/mol =14,2 mol
3. Find det enkleste muldvarpeforhold
* Divider hvert antal mol med det mindste antal mol (7,14 i dette tilfælde):
* Kulstof:7,14 mol / 7,14 mol =1
* Brint:14,2 mol / 7,14 mol =2
4. Skriv den empiriske formel
* Den empiriske formel repræsenterer det enkleste hele talforhold mellem atomer i forbindelsen.
* Den empiriske formel for denne kulbrinte er CH₂ .
 Varme artikler
Varme artikler
-
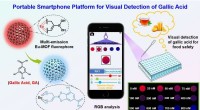 Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute
Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute -
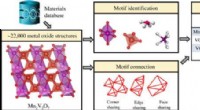 Struktur motiv-centreret læringsramme for uorganiske krystallinske systemerEkstraktion af strukturmotivinformation i uorganiske krystallinske forbindelser (metaloxider) og generering af globale motivrepræsentationer ved hjælp af motivmiljømatrixen. Kredit: Videnskab fremskri
Struktur motiv-centreret læringsramme for uorganiske krystallinske systemerEkstraktion af strukturmotivinformation i uorganiske krystallinske forbindelser (metaloxider) og generering af globale motivrepræsentationer ved hjælp af motivmiljømatrixen. Kredit: Videnskab fremskri -
 Fosforholdigt lipidmolekyle samler sig selv til en kubisk strukturKunstnerindtryk af de observerede fosfolipidterninger. Molekylerne er så tæt pakket, at membranen næsten ikke kan bøjes, resulterer i den kubiske form. Kredit:Moser Grafisk Design moser.ch For før
Fosforholdigt lipidmolekyle samler sig selv til en kubisk strukturKunstnerindtryk af de observerede fosfolipidterninger. Molekylerne er så tæt pakket, at membranen næsten ikke kan bøjes, resulterer i den kubiske form. Kredit:Moser Grafisk Design moser.ch For før -
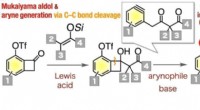 En dejlig reaktiv ring til det:Nye syntetiske veje til forskellige aromatiske forbindelserMukaiyama aldol-reaktionen af 6-(triflyloxy)benzocyclobutenoner med ketensilylacetaler og efterfølgende generering af aryner af γ-aryl-β-ketoester-type fra resulterende 6-(triflyloxy)benzocyclobuten
En dejlig reaktiv ring til det:Nye syntetiske veje til forskellige aromatiske forbindelserMukaiyama aldol-reaktionen af 6-(triflyloxy)benzocyclobutenoner med ketensilylacetaler og efterfølgende generering af aryner af γ-aryl-β-ketoester-type fra resulterende 6-(triflyloxy)benzocyclobuten


