Stærke vs. svage syrer:En omfattende guide til syrestyrke
1. Forstå definitionerne:
* Stærk syre: En syre, der ioniserer (donerer protoner, H+) fuldstændigt i opløsning. Dette betyder, at stort set alle syremolekylerne bryder sammen til ioner.
* Svag syre: En syre, der kun delvist ioniserer i opløsning. Kun en lille del af syremolekylerne donerer protoner.
2. Nøgleindikatorer:
* Ioniseringskonstant (Ka): Denne værdi kvantificerer omfanget af ionisering for en svag syre.
* Stærke syrer har meget store Ka-værdier (normalt> 1). Dette indikerer en høj grad af ionisering.
* Svage syrer har små Ka-værdier (normalt <1). Dette indikerer en lav grad af ionisering.
* pH: En stærk syre vil have en meget lav pH (indikerer høj surhedsgrad), mens en svag syre vil have en højere pH.
* Almindelig syreliste: Der er et par stærke syrer, som du bør huske. Disse er altid stærke:
* HCl (saltsyre)
* HBr (brintebrintesyre)
* HI (hydrojodsyre)
* HNO3 (salpetersyre)
* H2SO4 (svovlsyre)
* HClO4 (perchlorsyre)
3. Praktiske overvejelser:
* Kemisk formel: Tilstedeværelsen af visse grupper i et molekyle kan give dig et hint. For eksempel er carboxylsyrer (R-COOH) typisk svage syrer.
* Eksperiment: Du kan teste ledningsevnen af en syreopløsning. En stærk syre vil lede elektricitet meget bedre end en svag syre på grund af dens højere koncentration af ioner.
Eksempel:
* Saltsyre (HCl): Dette er en stærk syre. Det ioniserer fuldstændigt i opløsning, hvilket betyder, at stort set alle HCl-molekylerne dissocierer i H+ og Cl-ioner. Dens Ka-værdi er meget stor.
* Eddikesyre (CH3COOH): Dette er en svag syre. Kun en lille del af eddikesyremolekylerne donerer protoner (H+) i opløsning. Dens Ka-værdi er lille (ca. 1,8 x 10^-5).
Vigtig bemærkning: Udtrykkene "stærk" og "svag" henviser til omfanget af ionisering, ikke surhedsgraden. En stærk syre kan være stærkt koncentreret og derfor meget ætsende, men en svag syre kan også være ætsende, hvis den er koncentreret nok.
 Varme artikler
Varme artikler
-
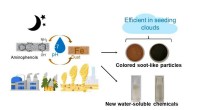 Ny kemi opstår, når støv møder forureningRepræsentation af forureningshændelser, hvor mineralstøv og biomassebrændende røg blandes. Kredit:Hind Al-Abadleh Det er en ny kemi fundet at finde sted i en skydråbe, en våd aerosol eller på overf
Ny kemi opstår, når støv møder forureningRepræsentation af forureningshændelser, hvor mineralstøv og biomassebrændende røg blandes. Kredit:Hind Al-Abadleh Det er en ny kemi fundet at finde sted i en skydråbe, en våd aerosol eller på overf -
 Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat
Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat -
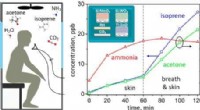 Bærbar enhed til at snuse ud fangede menneskerKredit:American Chemical Society Det første trin efter bygninger kollapsede fra et jordskælv, bombning eller anden katastrofe er at redde mennesker, der kunne blive fanget i murbrokkerne. Men at f
Bærbar enhed til at snuse ud fangede menneskerKredit:American Chemical Society Det første trin efter bygninger kollapsede fra et jordskælv, bombning eller anden katastrofe er at redde mennesker, der kunne blive fanget i murbrokkerne. Men at f -
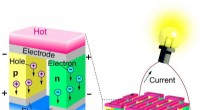 Flere halvleder type switch til at øge termoelektrisk konvertering af spildvarmeTinmonoselenid (SnSe), når dopet med antimon (Sb), kan danne en egnet kandidat til design af termoelektriske konverteringselementer (p-n-forbindelsesenhed). Kredit:Tokyo Tech I de seneste år, ener
Flere halvleder type switch til at øge termoelektrisk konvertering af spildvarmeTinmonoselenid (SnSe), når dopet med antimon (Sb), kan danne en egnet kandidat til design af termoelektriske konverteringselementer (p-n-forbindelsesenhed). Kredit:Tokyo Tech I de seneste år, ener


