Forståelse af valenselektroner:kemiske egenskaber og reaktivitet
* Kemisk binding: Valenselektroner er de yderste elektroner og er involveret i at danne kemiske bindinger med andre atomer. De kan deles (kovalente bindinger) eller overføres (ioniske bindinger) for at opnå en stabil elektronkonfiguration.
* Reaktivitet: Atomer med færre valenselektroner (tættere på en fuld ydre skal) har en tendens til at være mere reaktive og søger at vinde eller miste elektroner for at opnå stabilitet. Atomer med en fuld ydre skal (som ædelgasser) er ikke-reaktive.
* Typer af obligationer: Antallet af valenselektroner dikterer de typer bindinger et atom kan danne. For eksempel har grundstoffer med 1 eller 2 valenselektroner tendens til at danne ionbindinger, mens grundstoffer med 4 eller flere valenselektroner ofte danner kovalente bindinger.
* Oxidationstilstand: Antallet af valenselektroner påvirker et atoms oxidationstilstand, som beskriver dets ladning i en forbindelse.
Kort sagt, valenselektroner er nøglespillere i, hvordan atomer interagerer med hinanden, driver kemiske reaktioner og former verden omkring os.
 Varme artikler
Varme artikler
-
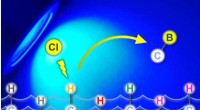 Ny tilgang inden for organisk kemi gør det muligt at tilføje bor til molekyler med høj præcisionEn simpel chloridkatalysator muliggør selektiv CH-borylering under milde fotokemiske forhold. Kredit:University of Bristol Et hovedmål inden for organisk syntese er at udvikle effektive reaktioner
Ny tilgang inden for organisk kemi gør det muligt at tilføje bor til molekyler med høj præcisionEn simpel chloridkatalysator muliggør selektiv CH-borylering under milde fotokemiske forhold. Kredit:University of Bristol Et hovedmål inden for organisk syntese er at udvikle effektive reaktioner -
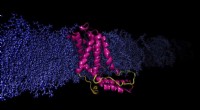 Undersøgelse afslører metodebegrænsninger til bestemmelse af proteinstrukturBeregningsmodel YidC2 protein indlejret cellemembran. Den modellerede sløjfe (gul), mangler i røntgenkrystalstrukturen, er afgørende for stabilisering af protein. Kredit:Sogol Moradi En ny undersø
Undersøgelse afslører metodebegrænsninger til bestemmelse af proteinstrukturBeregningsmodel YidC2 protein indlejret cellemembran. Den modellerede sløjfe (gul), mangler i røntgenkrystalstrukturen, er afgørende for stabilisering af protein. Kredit:Sogol Moradi En ny undersø -
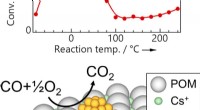 Ultraeffektiv fjernelse af kulilte ved hjælp af guld nanopartikler på en molekylær støtteNy katalysator bestående af guldnanopartikler understøttet på et Keggin-type polyoxometalat (POM) med et cæsiumsalt. Strukturen viste høj aktivitet og stabilitet for CO-oxidation; spormængder af vand
Ultraeffektiv fjernelse af kulilte ved hjælp af guld nanopartikler på en molekylær støtteNy katalysator bestående af guldnanopartikler understøttet på et Keggin-type polyoxometalat (POM) med et cæsiumsalt. Strukturen viste høj aktivitet og stabilitet for CO-oxidation; spormængder af vand -
 Sådan bruges antistoffer til at kontrollere kemiske reaktionerKunstnerisk fremstilling af to antistoffer, der udløser to kemiske reaktioner. Kredit:Oscar Melendre Hoyos I en samarbejdsindsats har en gruppe internationale forskere for nylig demonstreret en må
Sådan bruges antistoffer til at kontrollere kemiske reaktionerKunstnerisk fremstilling af to antistoffer, der udløser to kemiske reaktioner. Kredit:Oscar Melendre Hoyos I en samarbejdsindsats har en gruppe internationale forskere for nylig demonstreret en må
- SCRIM:En innovativ metode til 3-D betonprint
- Ekstreme vejrforhold og klimaændringer tegner sig for 40 % af den globale variabilitet i hvedeprodu…
- Forskerhold udvikler materiale til at adskille olie og vand til miljøsanering og spildevandsrensnin…
- Overfladebølger kan hjælpe nanostrukturerede enheder med at holde sig kølige
- Velfærdsbetingelser er ineffektive, siger forfattere af større undersøgelse
- De 97 km mellem Kina og beherskelsen af Mekong


