Nitrogenchlorid (NCl₃):Forståelse af dets polaritet
* Molekylær geometri: NCl3 har en trigonal pyramideform. Nitrogenatomet er i centrum, med tre kloratomer knyttet og et ensomt elektronpar på nitrogenet.
* Elektronegativitetsforskel: Klor er mere elektronegativt end nitrogen. Det betyder, at kloratomerne trækker de delte elektroner i N-Cl-bindingerne tættere på sig selv, hvilket skaber partielle negative ladninger (δ-) på kloratomerne og en partiel positiv ladning (δ+) på nitrogenatomet.
* Asymmetrisk afgiftsfordeling: De tre polære N-Cl-bindinger og det enlige par på nitrogenatomet ophæver ikke hinanden. Dette skaber et netto dipolmoment i molekylet, der peger mod kloratomerne.
På grund af de polære N-Cl-bindinger og den asymmetriske ladningsfordeling er NCl3 derfor et polært molekyle.
 Varme artikler
Varme artikler
-
 Rheostat identificeret, der hjælper med at regulere celledød versus overlevelsesbeslutningerForfattere Richard Kriwacki, PhD, og Aaron Phillips, PhD, identificeret, hvordan en ustruktureret eller iboende forstyrret region (IDR) i Bcl-xL giver større fleksibilitet til overvågning af forhold o
Rheostat identificeret, der hjælper med at regulere celledød versus overlevelsesbeslutningerForfattere Richard Kriwacki, PhD, og Aaron Phillips, PhD, identificeret, hvordan en ustruktureret eller iboende forstyrret region (IDR) i Bcl-xL giver større fleksibilitet til overvågning af forhold o -
 Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse,
Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse, -
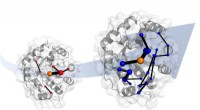 Forståelse af enzymudvikling baner vejen for grøn kemiLaboratorieudvikling af et designerenzym gør det til en meget bedre katalysator. Simuleringer viser, at evolutionen gør dette ved at indføre netværk af aminosyrer. Disse netværk lover at være skabelon
Forståelse af enzymudvikling baner vejen for grøn kemiLaboratorieudvikling af et designerenzym gør det til en meget bedre katalysator. Simuleringer viser, at evolutionen gør dette ved at indføre netværk af aminosyrer. Disse netværk lover at være skabelon -
 Differentiering af alkoholer fra alkener i laboratoriet:en praktisk vejledningThinkstock/Stockbyte/Getty Images En alkohol indeholder en hydroxyl (-OH) funktionel gruppe, hvorimod en alken er defineret af en carbon-carbon dobbeltbinding. Hver funktionel gruppe deltager i forsk
Differentiering af alkoholer fra alkener i laboratoriet:en praktisk vejledningThinkstock/Stockbyte/Getty Images En alkohol indeholder en hydroxyl (-OH) funktionel gruppe, hvorimod en alken er defineret af en carbon-carbon dobbeltbinding. Hver funktionel gruppe deltager i forsk


