Ædelgasser:hvorfor de ikke danner kemiske bindinger
Her er hvorfor:
* Fuld Valence Shells: Ædelgasser har en fuldstændig yderste elektronskal (også kendt som valensskallen). Dette betyder, at de har en stabil elektronkonfiguration og ikke behøver at vinde eller miste elektroner for at opnå en fuld skal.
* Lav reaktivitet: Deres stabile elektronkonfiguration gør dem meget ureaktive. De danner ikke let bånd med andre elementer.
Eksempler på ædelgasser omfatter:
* Helium (han)
* Neon (Ne)
* Argon (Ar)
* Krypton (Kr)
* Xenon (Xe)
* Radon (Rn)
Mens man engang troede, at ædelgasser var fuldstændig inerte, har forskere opdaget, at nogle ædelgasser kan danne forbindelser under specifikke forhold, især med stærkt elektronegative elementer som fluor. Imidlertid er disse forbindelser generelt meget ustabile.
Sidste artikelAmmoniak:En ikke-metallisk basisopløsning forklaret
Næste artikelOxidationstal af nitrogen og ilt i NO:En trin-for-trin guide
 Varme artikler
Varme artikler
-
 Bygninger:Det ubrydelige båndORNL-forskere producerede selvhelbredende og meget klæbende elastomerer, beviser, at de reparerer sig selv under omgivende forhold og under vandet. Kredit:ORNL/U.S. Institut for Energi Forskere ve
Bygninger:Det ubrydelige båndORNL-forskere producerede selvhelbredende og meget klæbende elastomerer, beviser, at de reparerer sig selv under omgivende forhold og under vandet. Kredit:ORNL/U.S. Institut for Energi Forskere ve -
 Superstrong Al -legeringer kan ændre fremstillingsprocesser til biler, rumfartsudstyrPå dette bilede, Qiang Li laver et afsætningsprogram på den operationelle computer, og Yifan Zhang indlæser prøver i et sputterkammer for at forberede højstyrke Al-legeringsbelægninger. Kredit:Purdue
Superstrong Al -legeringer kan ændre fremstillingsprocesser til biler, rumfartsudstyrPå dette bilede, Qiang Li laver et afsætningsprogram på den operationelle computer, og Yifan Zhang indlæser prøver i et sputterkammer for at forberede højstyrke Al-legeringsbelægninger. Kredit:Purdue -
 Lysere fleksibel elektroluminescerende film ved at adoptere øjenstruktur fra natlige dyrStruktur og karakteristika af elektroluminescerende anordning ved hjælp af rekursiv reflektionsstruktur. Strukturer (a~e) og betragtningsvinkelkarakteristika (f) af en elektroluminescerende enhed, der
Lysere fleksibel elektroluminescerende film ved at adoptere øjenstruktur fra natlige dyrStruktur og karakteristika af elektroluminescerende anordning ved hjælp af rekursiv reflektionsstruktur. Strukturer (a~e) og betragtningsvinkelkarakteristika (f) af en elektroluminescerende enhed, der -
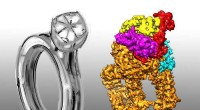 Team rapporterer diamantringarkitektur af et proteinkompleksNuA4 cryo-EM-strukturen ligner en diamantring. Kredit:USTC NuA4/Tip60, et kompleks med diamantringarkitektur, er påkrævet for lovgivnings- og reparationsprocesser. Prof. CAI Gang og Prof. Jacques
Team rapporterer diamantringarkitektur af et proteinkompleksNuA4 cryo-EM-strukturen ligner en diamantring. Kredit:USTC NuA4/Tip60, et kompleks med diamantringarkitektur, er påkrævet for lovgivnings- og reparationsprocesser. Prof. CAI Gang og Prof. Jacques
- Fifth Grade Math Fair Projekter
- Er fluor en leder af varme?
- Hvad er den mest almindelige enhed, der bruges til at måle energi fra biologiske systemer?
- Kan vækst bruges til at producere energi?
- Hvert øjeblik med ultrahurtig kemisk binding fanget på film
- Forskere udvikler den første AI-baserede metode til at datere arkæologiske rester


