Er fluor en leder af varme?
* ikke -metal: Fluor er et ikke -metalelement, og ikke -metaller er generelt dårlige ledere af varme.
* kovalent binding: Fluor findes som et diatomisk molekyle (F2) med stærke kovalente bindinger. Disse bindinger holder elektronerne tæt, hvilket gør det vanskeligt for varmeenergi at overføre gennem materialet.
* gasformig tilstand: Ved stuetemperatur er fluor en gas. Gasser er generelt dårlige ledere af varme, fordi deres molekyler er langt fra hinanden og har svage interaktioner.
I modsætning til fluor er metaller fremragende ledere af varme på grund af deres frit bevægende elektroner.
Sidste artikelLysfarven, der udsendes af et atom, er mest relateret til?
Næste artikelHvad kan måle væske?
 Varme artikler
Varme artikler
-
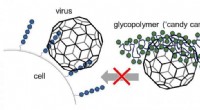 Kunstige slikstokke til at blokere viraDe kunstigt fremstillede glycomimetika (grønne) binder sig til viras bindingssteder, som vira normalt bruger til at binde til sukkerarter (blå) på celleoverfladen. Kredit:L. Hartmann, M. Schelhaas
Kunstige slikstokke til at blokere viraDe kunstigt fremstillede glycomimetika (grønne) binder sig til viras bindingssteder, som vira normalt bruger til at binde til sukkerarter (blå) på celleoverfladen. Kredit:L. Hartmann, M. Schelhaas -
 En grundlæggende mangel i luftforureningsmodellerKredit:CC0 Public Domain Forskere fra Københavns Universitet har opdaget et overraskende fænomen i en proces, hvorved visse gasmolekyler producerer skadelige partikler. Virkningen af dette fænom
En grundlæggende mangel i luftforureningsmodellerKredit:CC0 Public Domain Forskere fra Københavns Universitet har opdaget et overraskende fænomen i en proces, hvorved visse gasmolekyler producerer skadelige partikler. Virkningen af dette fænom -
 Forskere tuner materialers farve og termiske egenskaber separatDe visuelle og termiske egenskaber af polyethylen kan justeres til at producere farverige film med en bred vifte af varme-udstrålende egenskaber. Kredit:Felice Frankel Farven på et materiale kan o
Forskere tuner materialers farve og termiske egenskaber separatDe visuelle og termiske egenskaber af polyethylen kan justeres til at producere farverige film med en bred vifte af varme-udstrålende egenskaber. Kredit:Felice Frankel Farven på et materiale kan o -
 Additiv fremstilling af multifunktionelle deleSystem til Multi Material Jetting af højtydende komponenter med kombinerede egenskaber eller funktioner. Kredit:Fraunhofer IKTS Additiv fremstilling er i øjeblikket en af de vigtigste tendenser
Additiv fremstilling af multifunktionelle deleSystem til Multi Material Jetting af højtydende komponenter med kombinerede egenskaber eller funktioner. Kredit:Fraunhofer IKTS Additiv fremstilling er i øjeblikket en af de vigtigste tendenser
- Er der forskellige ord for syrer og alkali?
- Kodning og teknologiske færdigheder hjælper flygtninge og lavindkomstsamfund til at få succes
- Kæmpemuslinger fortæller historien om tidligere tyfoner
- Når den sydlige halvkugle er vippet mod sol, hvad sker der?
- Opbygning af en selvbærende robot fra e-skrot ved hjælp af vedvarende energi
- Holder affaldet, hvor det hører hjemme:Kornstørrelsen forklarer, hvordan brugt nukleart brændsel …


