Støkiometri:Beregning af produktudbytte fra reaktanter
1. Afbalanceret kemisk ligning:
* Det første skridt er at have en afbalanceret kemisk ligning for reaktionen. Denne ligning fortæller dig det nøjagtige antal mol af hver reaktant og produkt involveret i reaktionen. For eksempel:
* 2H2 + O2 -> 2H20
* Denne ligning fortæller os, at 2 mol hydrogengas (H₂) reagerer med 1 mol iltgas (O₂) og producerer 2 mol vand (H₂O).
2. Muldvarpeforhold:
* Koefficienterne i den afbalancerede ligning repræsenterer molforholdet mellem reaktanter og produkter. I eksemplet ovenfor er molforholdet mellem H2 og H2O 2:2, hvilket forenkler til 1:1. Det betyder, at for hver 1 mol H₂, der forbruges, produceres 1 mol H₂O.
3. Konvertering af masse til mol:
* Vi arbejder ofte med masser af reaktanter i stedet for muldvarpe. For at bruge støkiometri skal du konvertere massen af reaktanten til mol ved hjælp af dens molære masse.
* Molær masse er massen af et mol af et stof. Du kan finde det i det periodiske system.
4. Beregning af mol af produkt:
* Ved hjælp af molforholdet fra den balancerede ligning kan du beregne antallet af mol produkt, der vil blive dannet ud fra det givne antal mol reaktant.
* For eksempel, hvis du har 3 mol H₂, vil du producere 3 mol H₂O, fordi molforholdet er 1:1.
5. Konvertering af mol til masse:
* Endelig kan du konvertere mol produkt tilbage til gram ved hjælp af dets molære masse.
Eksempel:
Lad os sige, at du vil beregne massen af vand produceret af 10 gram brintgas.
1. Balanceret ligning: 2H2 + O2 -> 2H20
2. Moler H2:
* Molær masse af H₂ =2 g/mol
* Mol H₂ =10 g / 2 g/mol =5 mol
3. Moler H2O:
* Molforholdet mellem H2 og H2O er 1:1
* Mol H2O =5 mol (H2) x (1 mol H2O / 1 mol H2) =5 mol
4. Masse af H₂O:
* Molær masse af H2O =18 g/mol
* Masse af H2O =5 mol x 18 g/mol =90 g
Derfor vil 10 gram brintgas producere 90 gram vand.
Nøglepunkter:
* Støkiometri er baseret på loven om bevarelse af masse, som siger, at stof ikke kan skabes eller ødelægges i en kemisk reaktion.
* Den afbalancerede kemiske ligning er afgørende for støkiometriske beregninger.
* Støkiometri giver os mulighed for at forudsige mængden af produkt, der kan dannes ud fra en given mængde reaktant, som er afgørende for kemisk syntese og analyse.
 Varme artikler
Varme artikler
-
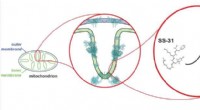 Forskere udforsker potentiel behandling for mitokondriesygdommeEt diagram, der viser SS-31, et peptid, eller kort kæde af aminosyrer, der let trænger ind i kroppens celler. SS-31 bliver støvet op af mitokondrier og smyger sig ind mod de indre vægge, hvor det skær
Forskere udforsker potentiel behandling for mitokondriesygdommeEt diagram, der viser SS-31, et peptid, eller kort kæde af aminosyrer, der let trænger ind i kroppens celler. SS-31 bliver støvet op af mitokondrier og smyger sig ind mod de indre vægge, hvor det skær -
 En ny måde at direkte omdanne metan til methanol ved hjælp af guld-palladium nanopartiklerRepræsentative HAADF-billeder og partikelstørrelsesfordelinger for den ikke-understøttede AuPd-PVP-sol i frisk (A til C) og efter en CH4-oxidationsreaktion (D til F). Kredit:Graham J. Hutchings og Chr
En ny måde at direkte omdanne metan til methanol ved hjælp af guld-palladium nanopartiklerRepræsentative HAADF-billeder og partikelstørrelsesfordelinger for den ikke-understøttede AuPd-PVP-sol i frisk (A til C) og efter en CH4-oxidationsreaktion (D til F). Kredit:Graham J. Hutchings og Chr -
 En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der
En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der -
 Video:Kan Google hjælpe dig med at få pletterne ud?Kredit:The American Chemical Society Plettet din skjorte, men har du ikke tid til en spin-cyklus? Din første impuls er sandsynligvis at piske din telefon ud og begynde at google. Men hvor pålid
Video:Kan Google hjælpe dig med at få pletterne ud?Kredit:The American Chemical Society Plettet din skjorte, men har du ikke tid til en spin-cyklus? Din første impuls er sandsynligvis at piske din telefon ud og begynde at google. Men hvor pålid
- Hvilken kategori af biomolekyler inkluderer sukker og stivelse?
- Undersøgelse advarer om, at slangesvampesygdom kan være en global trussel
- Undersøgelse:Målinger af lærernes præstationer kan straffe sorte undervisere
- Hvad bruges kemikaliet til at gøre celler lettere at se?
- Hvordan får Hubble -teleskopet information nede på jorden?
- Hvilke roller spiller proteiner i organismer?


