Bor-nitrogenbinding:Kovalent binding forklaret
Her er hvorfor:
* Elektronegativitet: Bor har en elektronegativitet på 2,04, mens nitrogen har en elektronegativitet på 3,04. Forskellen i elektronegativitet er signifikant, hvilket indikerer, at nitrogen tiltrækker elektroner stærkere end bor.
* Deling af elektroner: I stedet for at det ene atom fuldstændigt tager en elektron fra det andet, deler bor og nitrogen elektroner for at danne en stabil binding. Denne deling af elektroner er den definerende karakteristik af en kovalent binding.
Specifikt danner bor og nitrogen ofte en koordinat kovalent binding , hvor et atom (i dette tilfælde nitrogen) giver begge elektroner til det delte par.
Eksempler:
* Borazin (B3N3H6): Denne forbindelse kaldes ofte "uorganisk benzen" på grund af dens strukturelle lighed med benzen. Den indeholder alternerende bor- og nitrogenatomer forbundet med kovalente bindinger.
* Boronitrid (BN): Dette materiale findes i forskellige former, herunder sekskantet bornitrid (svarende til grafit) og kubisk bornitrid (svarende til diamant). Bindingerne mellem bor og nitrogen i disse strukturer er også kovalente.
 Varme artikler
Varme artikler
-
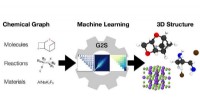 Fra kemiske grafer til strukturerMaskinlæringsmodellen Graph2Structure bruger grafer af kemiske forbindelser (venstre) til at forudsige deres 3D-koordinater (højre). Kredit:Dominik Lemm, Universitetet i Wien 3D-konfigurationer af
Fra kemiske grafer til strukturerMaskinlæringsmodellen Graph2Structure bruger grafer af kemiske forbindelser (venstre) til at forudsige deres 3D-koordinater (højre). Kredit:Dominik Lemm, Universitetet i Wien 3D-konfigurationer af -
 Ny kobberbelægning kunne blive den næste superbug fighterKredit:Pixabay/CC0 Public Domain En ny kobberbelægning, der dræber bakterier hurtigere og i større mængder end de nuværende formuleringer, kan snart være tilgængelig for hospitaler og andre højtraf
Ny kobberbelægning kunne blive den næste superbug fighterKredit:Pixabay/CC0 Public Domain En ny kobberbelægning, der dræber bakterier hurtigere og i større mængder end de nuværende formuleringer, kan snart være tilgængelig for hospitaler og andre højtraf -
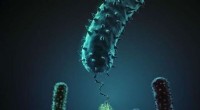 Bakteriel adhæsion in vitro og in silicoDenne figur viser, hvordan stafylokokker adhæsionsprotein (i grønt) interagerer med dets beslægtede peptidligand (rød). Kredit:H. Gaub, LMU München Ludwig-Maximilians-Universitaet (LMU) forskere
Bakteriel adhæsion in vitro og in silicoDenne figur viser, hvordan stafylokokker adhæsionsprotein (i grønt) interagerer med dets beslægtede peptidligand (rød). Kredit:H. Gaub, LMU München Ludwig-Maximilians-Universitaet (LMU) forskere -
 Beregning af ioniske tiltrækningskræfter ved hjælp af Coulombs lovAf Jack Brubaker Opdateret 24. marts 2022 Når metaller og ikke-metaller danner forbindelser, donerer metalatomer elektroner til ikke-metalatomer. Metalatomerne bliver positivt ladede ioner, mens ikk
Beregning af ioniske tiltrækningskræfter ved hjælp af Coulombs lovAf Jack Brubaker Opdateret 24. marts 2022 Når metaller og ikke-metaller danner forbindelser, donerer metalatomer elektroner til ikke-metalatomer. Metalatomerne bliver positivt ladede ioner, mens ikk


